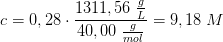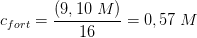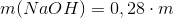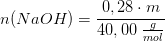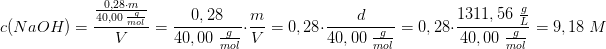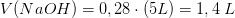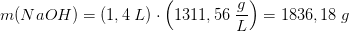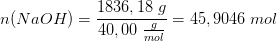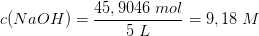Kemi
Beregning af NaOH konc opløst i vand
Opløser man 5 liter 28% NaOH i 80 liter vand får man en NaOH-opløsning på 2%.
Er der nogen der kan vise mig beregningen?
På forhånd tak
Peter
Svar #1
01. juli 2014 af mathon
28% NaOH (aq) har densiteten 1,31156 g/mL (opslag og ekstrapolering)
Svar #2
01. juli 2014 af mathon
eller
opløsningen fortyndes
i forholdet
1 : 16
hvorfor
den nye masseprocent
bliver
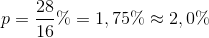
Svar #3
12. juli 2014 af Martin84a (Slettet)
Jeg tillader mig lige at genoplive dette spørgsmål. Men er det ikke en underlig måde at stille et spørgsmål på, og det er meget tvetydigt.
En NaOH opløsning på 2% er alt der skrives, men 2% af hvad. Masseprocent, volumenprocent, antal molekyler/antal mol...ja man kunne også smide densitetsprocenten derinde. Er der en uskrevet reglen et eller andet sted, at når der står "x% af en opløsning", så menes der fx altid af massen?
Svar #4
12. juli 2014 af mathon
densiteten af 28% NaOH er 1,31156 g/mL.
Hvis masseprocent:
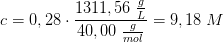
efter fortynding:
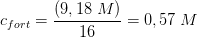
Skriv et svar til: Beregning af NaOH konc opløst i vand
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.