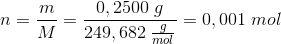Kemi
Masse (g) af CuSO4 5H2O
Hej mennesker.
Jeg står med følgende opgaveformulering: Beregn stofmængden (antal mol) af CuSO4 5H2O i de tre kolber.
Jeg nøjes med at smide oplysninger om kolbe 1 op, da jeg egentlig kun mangler en fremgangsmåde.
Kolbe 1 indeholder 0,2500 g CuSO4 5H2O.
Jeg er klar over, at jeg skal bruge formlen: n = m/M, og da jeg allerede har fundet M (250 g/mol), mangler jeg blot at finde ud af, hvordan i alverden jeg finder m.
Jeg har stirret mig helt blind på den her opgave og håber, at der er nogen, der kan give en hjælpende hånd. :)
Svar #1
20. september 2014 af mathon
M(CuSO4*5H2O) = M(CuSH10O9) = sum({1,1,10,9}*{63.546,32.065,1.008,15.999}) = 249,682 g/mol
Svar #2
20. september 2014 af Nojzy (Slettet)
D'oh, efter at have postet det her kan jeg selvfølgelig godt se, at opgaven allerede har givet mig 'm' i form af de 0,2500 g.
Tak for svaret, mathon, men det var lille 'm', jeg ledte efter og ikke stort 'M', som du vist har udregnet. :)
Svar #4
20. september 2014 af Nojzy (Slettet)
Tusind tak, det var også det resultat, jeg kom frem til.
Skriv et svar til: Masse (g) af CuSO4 5H2O
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.