Kemi
Ligevægtskonstant
Håber der er nogle der kan hjælpe med følgende opgave. Jeg har udregnet ligevægtskonstanten ved 298 K, men jeg er ikke sikker på om det er rigtigt. K = e-175200 J/mol / 8,314*298 K = 1,95*10-31
Vi ser på reaktionen: N2(g) + O2(g) → 2 NO(g)
Denne reaktion bevirker, at der er NO i udstødningsgassen fra biler og i røgen fra kraftværker og andre forbrændingsanlæg.
a) Beregn ligevægtskonstanten ved 298 K, ved 1500 K og ved 2000 K.
b) Røgens indhold af NO forøges, når forbrændingstemperaturen sættes op. Hvordan kan det forklares?
c) Røgen indeholder mere NO, når forbrændingsgasserne nedkøles hurtigt, end når de nedkøles relativt langsomt. Hvordan kan det forklares?
d) Nævn nogle skadevirkninger af at lukke NO ud i luften.
Svar #1
01. oktober 2014 af Heptan
Opgave: Basiskemi A http://gymportalen.dk/basiskemiaibog/14538
Jeg har ikke tjekket dit resultat, men du har brugt den rigtige formel
a) ved 1500 K og 2000 K, brug formlen herunder.

b) Det kan forklares ud fra ligevægtskonstanternes størrelse (mon ikke de bliver større og større? Brug a))
c) ????
d) NO er kraftigt reducerende. Brug evt. google.
Svar #3
02. oktober 2014 af Heptan
#2 Det vil være nemmere at undlade at beregne DeltaG-standard, og så bruge formlen i #1 istedet, da man skal bruge den alligevel, men nu har #0 jo allerede beregnet K ved 25 Co
Svar #4
02. oktober 2014 af Hippocampus (Slettet)
#3
Vil man ikke normalt slå værdierne for entalpi og entropi op i en databog? Jeg spørger af nysgerrighed, da jeg ikke har haft kemi A og dermed ikke har haft termodynamik. Jeg vil dog i gang med at læse på det for sjov - kan du anbefale nogle gode bøger?
Svar #5
02. oktober 2014 af Heptan
#4
Jo, det vil man
Har desværre ikke noget at anbefale, andet end en kemi A bog... eller evt. bare Formelsamlingen Kemi A. Jeg forstår ikke selv begreberne entropi og gibbs i detaljer, andet end at det har noget med "uorden" og "spontanitet" at gøre, p.t., men der ligger vist en masse matematik bag
Svar #6
02. oktober 2014 af Hippocampus (Slettet)
#5
Tak for svaret.
Så værdierne for S og H i #1 vil man blot slå op til udregningen?
Svar #7
02. oktober 2014 af Heptan
Man skal beregne 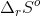 og
og 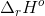 ud fra de værdier man finder i databogen (som er
ud fra de værdier man finder i databogen (som er 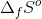 og
og 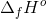 )
)
Svar #10
02. oktober 2014 af Heptan
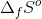 er den værdi der for hver partikel står i databogen.
er den værdi der for hver partikel står i databogen. 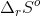 er den værdi der beregnes for netop den aktuelle reaktion, altså summen af
er den værdi der beregnes for netop den aktuelle reaktion, altså summen af 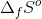 -værdierne.
-værdierne.
Svar #11
02. oktober 2014 af Hippocampus (Slettet)
#10
Jep, det kan jeg se i svaret #8. Jeg var blot igang med at skrive #9, mens du svarede i #8.
Tak for svar alligevel dog.
Skriv et svar til: Ligevægtskonstant
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.


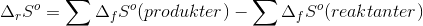
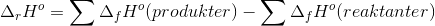
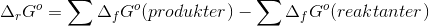
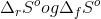 ?
?