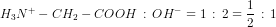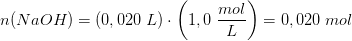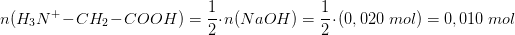Kemi
mængde NaOH
24. november 2014 af
UK343
-
Niveau: A-niveau
Hvordan finder jeg mængden af NaOH ved en titrering med 20,00 mL. NaOH er 1,000 M.
Jeg vil mene man skulle gange 0,020 L med 1,000 M, men ved resultatet skal give 0,010 mol.
Må man gange med en halv eller?
Titrereaktionen ser således ud:
H3O+ - CH2 - COOH + 2OH- --> H2N - CH2 - COO- + 2H2O
Svar #4
24. november 2014 af UK343
Jeg ved kun disse ting, som skrevet øverste, men er det fordi at stifmængdeforholdet er 1:2 også må jeg dividere med 2?
Skriv et svar til: mængde NaOH
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.



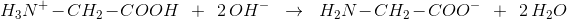
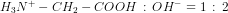
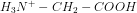
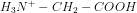 ved en titrering med 20,00 mL 1,000 M NaOH.
ved en titrering med 20,00 mL 1,000 M NaOH.