Kemi
Enzymreaktion
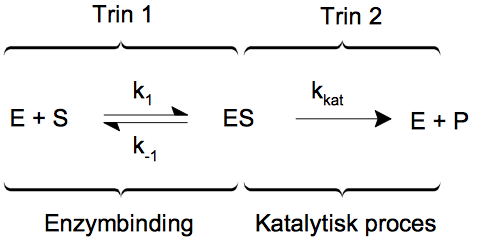
Hej, er der nogle dygtige mennekser, som ved hvorfor der ved trin 1 er ligevægtspil, mens der i trin 2 er en almindelig reaktionspil, og sidste trin, altså trejde trin også er ligevægtspile?
Svar #1
16. december 2014 af OliverGlue
Jeg ser ikke et trejde trin?
Trin 2 er også en ligevægt, men hastighedskonstanten for den tilbagegående reaktionn er ikke særlig stor, det er blot en approksimation - der gør det meget lettere at betragte enzymkinetik.
Svar #2
16. december 2014 af flygtighed (Slettet)
det er en model til at betragte enzymreaktioner.
det betyder, at først skal substrat og enzym bindes. det er en ligevægt mellem ES-kompleks og frit E og S, og da det er en ligevægt forløber det lige hurtigt i begge retninger.
det næste trin sker der omdannelse af ES til P + E. den er irreversibel. det er det hastighedsbegrænsende trin, og afgør altså hvor hurtig den enzymatiske reaktion forløber.
når man bruger f.eks. michaelis-menten modellen antager man at enzymreaktionen forløber sådan her :)
det er som nævnt i #1 en approksimation - en antagelse som man gør sig, som gør det nemmere at forstå enzymkinetik
Svar #3
17. december 2014 af Sneharusha (Slettet)
HOv, tror jeg sattte det forkerte billede ind, men det gør ikke så meget. Kan jeg spørge hvorfor det første trin er en ligevægt, mens trin 2, ikk er en almindelug reaktion?
Svar #4
17. december 2014 af Heptan
Analog:
Fysisk er det ret nemt at flække et æg, lave en omelet og spise den.
Men det er meget sværere at lave et æg af en omelet, som man lige har spist.
Det følger af termodynamikkens 2. lov, der siger at universet har en tendens til at få mere "uorden", altså det modsatte af perfekt orden.
__________________________
Tilsvarende er det nemt at have en ligevægt mellem et enzym og et substrat, der komplekserer, to stoffer der klæber sammen og dissocierer igen. Men når enzymet først har omdannet substratet (ofte kommer der flere produkter ud af det), så er det problematisk at sætte enzym og produkter sammen på den helt korrekte måde, og omdanne dem til substrat, ligesom det er svært at lave et æg af en omelet man har spist.
Det er ikke indlysende når man ser på et reaktionsskema, men man kan lave termodynamiske beregninger på, om reaktionen E + P → E + S er en spontant reaktion.
Svar #5
17. december 2014 af flygtighed (Slettet)
Igen; det er en måde at betagte enzym-mekanismer.
alting styres mod ligevægt. Nu siger vi det er en ligevægt mellem ES-kompleks og frit E og frit S, men forestil dig at enzymet er meget effektiv og hurtigt omdannes ES til frit E og frit P. så stiger mængden af frit E, og det vil forskyde
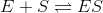
mod højre, dvs. der vil dannes mere ES-kompleks. Og igen vil ES-kompleks blive omdannet til frit E og P, som vil forårsage en forskydning af ligevægten igen. det er 'ønsket' om at opnå ligevægt som vil drive hele substrat-omdannelsen.
trin 2 er en alm. (enzym)-reaktion, ja. det er det hastighedsbestemmende trin for enzymet.
Skriv et svar til: Enzymreaktion
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.

