Bioteknologi
Blandinger - HÆÆÆLP!
Jeg har en opgave der lyder sådan:
Koncentreret ammonikavand har masseprocenten 25%. Densiteten af koncentreret ammoniakvand er 0,91 mg/ l. Vi vil fremstille 1 liter 2,0 M opløsning af ammoniak.
Spørgsmål:
Hvordan vil i lave opløsningen?
Er der nogen der kan hjælpe?
Svar #2
27. januar 2015 af StudyHard100 (Slettet)
Altså det er selve fremgangsmåden (dog ikke i detaljer)...
Svar #3
27. januar 2015 af mathon
Antal mol NH3 i 1 L 2,0 M NH3
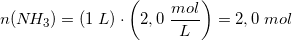
Massen heraf:
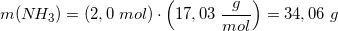
som fremstillet af 25 masseprocent NH3
kræver:
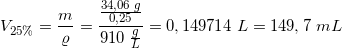
Den ønskede 1 L 2,0 M NH3 fremstilles ved i en 1 L kolbe at ihælde 149,7 mL 25% NH3-opløsning og efterfylde med demivand til mærket.
Svar #5
27. januar 2015 af StudyHard100 (Slettet)
Okay har prøvet at regne på det sidste led, men kan ikke se hvor du får 910 g/l fra?
I det sidste led har jeg for øvrigt brugt formlen: Cmasse% = masse (A) / masse (B) * 100%
Jeg får det til 136,24 ved at bruge den overstående formel
Svar #6
23. februar 2015 af Andersen11 (Slettet)
#5
Det er densiteten af koncentreret ammoniakvand, der nok i #0 skulle være
ρ = 0,91 kg/L = 910 g/L .
Skriv et svar til: Blandinger - HÆÆÆLP!
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.



