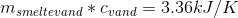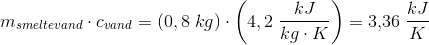Fysik
Specifik smeltevarme
Hej.
Hvis man skal beregne en temperatur, for en vandmængde ud fra følgende:
Hvis man smider 0,8 kg is med en temperatur på -20 C ned i en tønde med 10 L vand med en temperatur på 200 C.
Hvordan gør man så det? (har vedhæftet et billede af det jeg har forsøgt - men det giver ingen mening)
Svar #1
29. januar 2015 af mathon
opvarmning af is + smeltning af is + opvarmning af smeltevand = afkøling af tøndevand
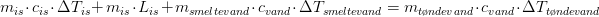
Svar #3
29. januar 2015 af Kim777 (Slettet)
Kan det passe at den samlede vandmængde i vandbaljen når isen er smeltet kun er faldet med 4 grader celcius?
Svar #7
29. januar 2015 af Kim777 (Slettet)
Kan du lige prøve at beregne det hvis vi siger følgende:
Vandbalje: 50 L med en temperatur på 200 °C.
Istap: 0,8 kg med en temperatur på -50 °C
?
Skriv et svar til: Specifik smeltevarme
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.




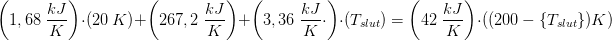
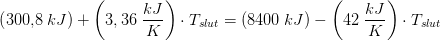
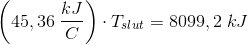
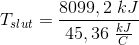
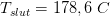
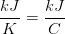
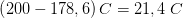
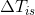 til at være 20 K
til at være 20 K