Kemi
Beregn koncentrationen når ligevægten har indstillet sig
01. februar 2015 af
Esterificering
-
Niveau: B-niveau
Hej SP, Opgaven handler om følgende ligevægt:
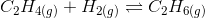
Ligevægtskonstanten Kc = 078M-1 ved temperaturen 900K
Reaktionen foregår i en beholder på 10L, der som startbetingelse indeholder 1,0mol C2H4 og 1,0mol H2 ved temperaturen 900K.
a) Opskriv reaktionsbrøken for ligevægten.
![K_{c}=\frac{\left [ C_{2}H_{6} \right ]}{\left [ C_{2}H_{4} \right ]\cdot\left [ H_{2} \right ]}](https://media.studieportalen.dk/images/equations/08TEWB1nNo3J0GE2Qpq6SA==.gif)
b) Beregn koncentrationen af de tre forbindelser, når ligevægten har indstillet sig.
(Det er her jeg har brug for hjælp)
Mvh. Tino
Skriv et svar til: Beregn koncentrationen når ligevægten har indstillet sig
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.







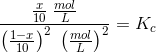
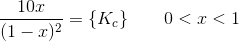
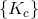 betyder talværdien af størrelsen
betyder talværdien af størrelsen