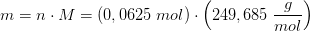Kemi
hensyn til krystalvand i stofmængdekoncentration?
Hej alle sammen. Hvordan tager jeg hensyn til kobbersulfat indeholder krystalvand i den opgave jeg har vedhæftet? Skal jeg bare medregne krystalvandet i den molare masse af stoffet, men så tænker jeg selv bare det bliver 0,125M CuSO4 inkl krystalvandet og ikke 0,125 ren CuSO4 ?
Jeg håber I kan hjælpe mig
Svar #2
12. marts 2015 af mathon
3 a)
Beregn antal nødvendige mol ren CuSO4.
Beregn den ækvivalente masse CuSO4•5H2O.
.
3 b)
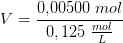
Svar #3
12. marts 2015 af 321bj (Slettet)
hvordan beregner jeg den ækvivalente masse CuSO4•5H2O ?
har fået det nødvnedige antal mol til:
n = c*V = 0,125M*0,5L = 0,0625
Skal jeg også bruge molarmassen af ren kobbersulfat = 159,62 g/mol ?
Svar #7
12. marts 2015 af 321bj (Slettet)
ok så jeg skal ikke bruge kobbersulfat uden krystalvand til noget ?
Svar #9
04. august 2015 af Soeffi
Opgavetekst:
3. Stoffet CuSO4·5H2O anvendes til at lave 500 mL 0,125 M CuSO4.
a) Beregn massen af CuSO4·5H2O, som skal bruges til opløsningen.
b) Hvor stort et volumen skal man afmåle af opløsningen, hvis man skal bruge 0,005 mol CuSO4?
Svar:
a) masse af CuSO4·5H2O = antal mol CuSO4·5H2O gange molmassen af CuSO4·5H2O. Antal mol CuSO4·5H2O = koncentration af CuSO4 gange rumfang af opløsning. Molmassen er 249,7 g/mol af kobbersulfat med 5 krystalvand. Dette giver: antal mol CuSO4·5H2O = 0,50 L · 0,125 mol/L = 0,0635 mol. Dvs. massen af CuSO4·5H2O = 0,0625 mol · 249,7 g/mol = 15,6 g.
b) Rumfang = antal mol CuSO4 divideret med koncentration af CUSO4 i opløsning = 0,005 mol/(0,125 mol/L) = 0,04 L = 40 mL.
Skriv et svar til: hensyn til krystalvand i stofmængdekoncentration?
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.