Kemi
Raktion md eddikesyre
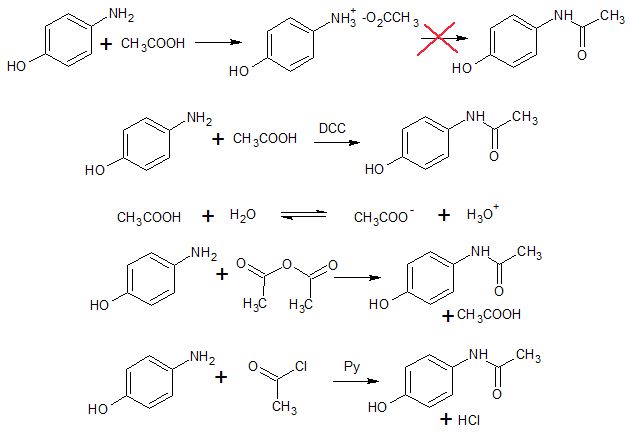
Hej. Jeg skal besvare et spørgsmål, der lyder på hvorfor 4-aminophenol kan reagere med eddikesyre, når paracetamol ikke kan.
Jeg har en idé om, at det måske er fordi paracetamol allerede har en carboxyl-gruppe (er det ikke det, det hedder?), men jeg forstår egentlig ikke helt hvorfor dette forhindrer den i at reagere med eddikesyren.
Er der nogen, der kan hjælpe?
Svar #1
31. marts 2015 af Heptan
Det hedder et amid. Aminer kan reagere med carboxylsyrer, hvis de først aktiveres med et passende reagens. Produktet er et amid. Reaktionen er analog med peptiddannelsen, der opbygger de proteiner vores krop bruger.
I paracetamol er amidet allerede blevet dannet, så amiddannelse kan ikke finde sted igen.I princippet kan der finde en esterdannelse sted, under de rette betingelser. Dvs. phenolen (-OH) kan reagere med carboxylsyren og danne en ester, men reaktionen er langsom og kræver de rette reaktionsbetingelser.
Svar #2
06. april 2015 af EnStuderende
Aha. Mange tak for det gode svar, og beklager at jeg har været så længe om at svare!
Det var det med esterdannelsen, jeg især lige manglede at høre. Men kommer produktet så til at se ud som følgende?

Svar #3
06. april 2015 af EnStuderende
Og hvorfor er reaktionen langsom?
Jeg tænker, at hvis nu 4-aminophenol og paracetamol var til stede begge to, så ville eddikesyren vel altid reagere med 4-aminophenol først fordi amingruppen er mere nukleofil en hydroxygruppen... men når al 4-aminophenol er brugt op, kan der så godt ske denne esterdannelse, og hvis ja, vil det så ikke formindske det teoretiske udbytte af paracetamol? Altså hvis det efterfølgende bliver omdannet til en ester mister man vel noget af det.
Endnu et spørgsmål... hvis OH-gruppen i phenol kan reagere med eddikesyren, hvorfor kan vand så ikke? Er det, fordi vands bindinger er for stærke, fordi det er dipol-dipol bindinger? Eller har det noget at gøre med hydrogenbindingerne?
Svar #4
06. april 2015 af EnStuderende
Bah, der skulle selvfølgelig ikke stå OH til sidst men resten af paracetamol-kæden..... Men du forstår vel, hvad jeg mener :-)
Sådan her.... og bliver restproduktet så dihydrogen? Eller er jeg helt på afveje?

Svar #5
06. april 2015 af Heptan
#2 Nej, hvis der sker en esterdannelse er det via OH-gruppen (phenolen).
#3 Reaktionen er ikke langsom hvis den bliver katalyseret.
Hvorfor skulle aminen være mere nukleofil end phenolen?
Jeg tænker, at hvis nu 4-aminophenol og paracetamol var til stede begge to, så ville eddikesyren vel altid reagere med 4-aminophenol først
Det er ikke så simpelt endda ... problemet her er, at der finder en konkurrerende reaktion sted (som vinder!). Det er syre/basereaktionen ... anilin er en base og eddikesyre er en syre, og når der er overført en proton får man en ammoniumion og ethanoat. Ethanoat er helt inert overfor substitutioner, så hvis du ser på en evt. øvelsesvejledning vil du måske opdage at der er tilsat nogle katalysatorer? (Ellers er det mig der tager fejl :P)
Endnu et spørgsmål... hvis OH-gruppen i phenol kan reagere med eddikesyren, hvorfor kan vand så ikke? Er det, fordi vands bindinger er for stærke, fordi det er dipol-dipol bindinger? Eller har det noget at gøre med hydrogenbindingerne?
Du spørger hvorfor vand ikke kan reagere med eddikesyre? Der er to grunde: Eddikesyre kan godt reagere med vand, men hvis du ser på substitutionsreaktionen ...
CH3COOH + H2O → CH3COOH + H2O
... ja, så vil det måske gå op for dig. Desuden sker der, igen, en sideløbende reaktion, altså syre/base reaktionen.
Svar #6
06. april 2015 af Heptan
#4
Hvis du ser på reaktionsskemaet, så mangler du et oxygenatom ... dvs. der dannes ikke H2, men H2O. Reaktionen er en kondensationsreaktion ligesom amiddannelsen. Desuden er der en enkeltbinding i H2!
Svar #7
06. april 2015 af EnStuderende
Hvorfor skulle aminen være mere nuklefoil end phenolen?
Det var noget min lærer sagde... 4-aminophenol kan i princippet reagere med både sin amingruppe og hydroxygruppe, men den reagerer først/mest/altid? med aminen først, fordi den er mere basisk (fordi nitrogen er mindre elektronegativ end oxygen) og mere nukleofil (dvs. den har højere pKs og er mere villig til at donere en elektron i en kemisk reaktion), hvorimod hydroxy-gruppen er mere sur.
Eller amingruppen er i hvert fald mere reaktiv....
Haha ja okay... :-)
Men hvis jeg nu har udregnet et teoretisk udbytte ud fra, hvor meget 4-aminophenol der tilsættes, er dette teoretiske udbytte så ikke "forkert" i praksis, da der jo finder esterdannelse sted?
Svar #8
06. april 2015 af EnStuderende
Men er der ikke kun 4 O'er? Hvor skulle O'et til H2O komme fra?
Svar #10
06. april 2015 af Heptan
Det var noget min lærer sagde... 4-aminophenol kan i princippet reagere med både sin amingruppe og hydroxygruppe, men den reagerer først/mest/altid? med aminen først, fordi den er mere basisk (fordi nitrogen er mindre elektronegativ end oxygen) og mere nukleofil (dvs. den har højere pKs og er mere villig til at donere en elektron i en kemisk reaktion), hvorimod hydroxy-gruppen er mere sur.
Det er sådan set rigtigt nok ... men hvis du blander ethansyre og 4-aminophenol, vil du ikke få noget paracetamol ... fordi der sker en syre/base reaktion. Netop fordi aminogruppen er en bedre base, vil hydroxygruppen istedet "vinde", især hvis solventet er surt eller basisk. Da phenolen er en syre, kan der dannes den meget nukleofile phenolation, som så vil dominere.
Hvad man istedet kan gøre er, at man kan bruge et opløsningsmiddel, som ikke er vand (for at undgå syre/base reaktioner), og et andet acetylingsmiddel end eddikesyre.
Svar #11
06. april 2015 af EnStuderende
Nårh ja, det er fordi det er en lidt anden reaktionsmekanisme jeg tænker på :-) Okay, nevermind, men tak!
Jeg skal bare lige være sikker: er produktet i #9 rigtig?
Svar #12
06. april 2015 af Heptan
#9 Ja (de tre vinkler i esteren er dog 120º)
#7
Men hvis jeg nu har udregnet et teoretisk udbytte ud fra, hvor meget 4-aminophenol der tilsættes, er dette teoretiske udbytte så ikke "forkert" i praksis, da der jo finder esterdannelse sted?
Det kommer an på reaktionsbetingelserne. Det teoretiske udbytte er jo altid "forkert" i praksis ... men det er rigtigt at den konkurrerende esterdannelse vil mindske udbyttet (spørgsmålet er så, hvor meget) ... det kan man så diskutere under sine fejlkilder. Hvis du laver en analyse af dit produkt, kan du jo undersøge hvor meget af esteren der er blevet dannet.
Svar #15
07. april 2015 af EnStuderende
Så der bliver smidt et H væk i eddikesyren, OH kommer væk fra phenol, og der bliver dannet vand + en bindingen mellem benzenringen og carboxylsyren?
Svar #16
07. april 2015 af Heptan
Godt tænkt, men den nye binding der bliver dannet er den mellem oxygen fra phenolen og carbonyl-carbonatomet i eddikesyre. Dvs. oxygen i H2O kommer fra eddikesyre (men som sagt, reaktionen finder ikke direkte sted mellem eddikesyre og 4-aminophenol).
Svar #20
07. april 2015 af EnStuderende
#19 Fedt! Mange tusind tak for hjælpen, det hele giver meget mere mening for mig nu :-)
Skriv et svar til: Raktion md eddikesyre
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.