Kemi
syrebase-kemi
Hej,
Er der en derude som kan hjælpe mig med at komme igang med denne opgave i kemi..
Jeg har vedhæftet opgaven som en pdf
På forhånd tak!
Svar #1
25. april 2015 af Heptan
a) Benyt formlen for densitet,
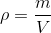
og isolér massen m
b) Nu kender du massen. Benyt
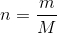
c) Nu kender du stofmængden. Benyt
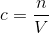
d) Udnyt at
![[NH_2^-]=[NH_4^+]](https://media.studieportalen.dk/images/equations/SRr7qyX-gDq0W8lu9LrSKQ==.gif)
og løs fx ligningen
![[NH_2^-]^2 =10^{-30}\ \textup{M}^2](https://media.studieportalen.dk/images/equations/sE7Cs7s6keFk4FQfczKuIQ==.gif)
e) Da du kender koncentrationen af NH4+ fra opg d), kan du nu beregne stofmængden, og dermed antallet af ammoniumioner i 5,0 mL flydende ammoniak:
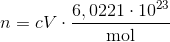
Svar #2
25. april 2015 af jens12234 (Slettet)
Mange tak! i a) skal jeg lave g/ml om til kg/l ik? skal vel have det om til L hvert fald, da volumen er 0,005 L?
Kan du også forklare hvad man skal i c) og d)?
Svar #4
27. april 2015 af jens12234 (Slettet)
Er der en som kan forklare mig e) lidt bedre? skal jeg sige n=c*V*6,0221*10^23
Skriv et svar til: syrebase-kemi
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.