Kemi
ligevægt mm.
Oxalsyre, (COOH)2, er en divalent syre med Ks1 = 10–1,27 M, dvs. ligevægtskonstanten for reaktionen: (COOH)2 ? H+ + HC2O4–
3a) Beregn [H+] og [(COOH)2] i en 0,250 M opløsning af oxalsyre, når der kun tages hensyn til ovennævnte ligevægt. (har jeg løst => [H+]=0,092M og [(COOH)2]=0,158M)
3b) Den anden syrestyrkekonstant for oxalsyre, Ks2, er ligevægtskonstanten for reaktionen: HC2O4– ? H+ + C2O42−. Ligevægtskonstanten er K = 10–5,54 M2 for reaktionen: (COOH)2 ? 2 H+ + C2O42−. Beregn Ks2. (har jeg løst = 5,4*10^-5)
3c) Opløselighedsproduktet for calciumoxalat, Ca(C2O4), er L = 2,32 · 10-9 M2. Opskriv reaktionsskemaet for den reaktion, der svarer til denne konstant, og beregn den masse (mg) af calciumoxalat, som kan opløses i 1,00 liter vand, når der ikke tages hensyn til oxalationens baseegenskaber. Molær masse/g·mol–1: Ca(C2O4): 128,1. (har jeg løst = 6,2mg)
3d) Calciumoxalat kan opløses helt eller delvist i syre i kraft af oxalationens baseegenskaber. Beregn ligevægtskonstanten, K´, for reaktionen: Ca(C2O4)(s) + 2 H+? Ca2+ + (COOH)2. Beregn [Ca2+] i den ligevægtsopløsning, der fremkommer, når overskud af fast calciumoxalat bringes i kontakt med en 1,00 M HCl-opløsning. <- denne har jeg brug for hjælp til :)
3e) En pufferopløsning fremstilles ved at opløse 4,052 g oxalsyre og 8,402 g natriumhydrogenoxalat, Na(HC2O4), i vand til 300 ml. Beregn de formelle koncentrationer af oxalsyre og hydrogenoxalat i opløsningen. Benyt pufferligningen til at forudsige opløsningens pH. Molær masse/g·mol–1: (COOH)2: 90,04; Na(HC2O4): 112,02. (harjeg løst => C(oxal) = 0,150 M, C(hydrog.oxalat) = 0,250 M, pH=1,49)
3f) Til 50,00 ml af en 0,500 M oxalsyre-opløsning i en 100-ml målekolbe tilsættes et ukendt rumfang 0,40 M natriumhydroxid, hvorefter der fortyndes til 100,0 ml. Efter omrystning måles opløsningens pH = 1,61. Beregn koncentrationen af hydrogenoxalat i opløsningen. <- denne har jeg brug for hjælp til :)
Skriv et svar til: ligevægt mm.
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.




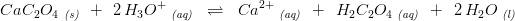
![\frac{\left [ Ca^{2+} \right ]\cdot \left [ H_2C_2O_4 \right ]}{\left [ H_3O^+ \right ]^2}=K{\, }'](https://media.studieportalen.dk/images/equations/hkPJW5UbqGhFdZUr65khGg==.gif)
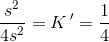
![\left [ Ca^{2+} \right ]\! \! :](https://media.studieportalen.dk/images/equations/W90Kn2LEcNfPt_hce5fLRQ==.gif)
![\frac{\left [ Ca^{2+} \right ]\cdot \left [ H_2C_2O_4 \right ]}{\left [ H_3O^+ \right ]^2}=\frac{1}{4}](https://media.studieportalen.dk/images/equations/Gd4qU33phySuxEJM-2NDEA==.gif)
![\left [ Ca^{2+} \right ]=\frac{1}{4}\cdot \frac{\left [ H_3O^+ \right ]^2}{\left [ H_2C_2O_4 \right ]}](https://media.studieportalen.dk/images/equations/GQMdEZJoo2Dyf-7IeKGH7A==.gif)
![\left [ Ca^{2+} \right ]=\frac{1}{4}\cdot \frac{(1{,}0\; M)^2}{0{,}5\; M }=0{,}5\; M](https://media.studieportalen.dk/images/equations/6mVp_BVVOCqO4bwmGTDHUw==.gif)
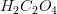 :
: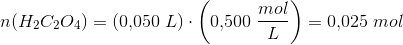
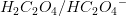
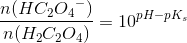
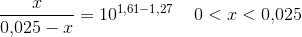
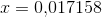
![\left [ HC_2{O_4}^{-} \right ]=\frac{n}{V}=\frac{0{,}017158\; mol}{0{,}100\; L}=0{,}172\; M](https://media.studieportalen.dk/images/equations/ZeyYX8r5RqzmjOuZJVGR0Q==.gif)
![\left [ Ca^{2+} \right ]=\frac{1}{4}\cdot \frac{\left [ H_3O^+ \right ]^2}{\left [ H_2C_2O_4 \right ]}=\frac{1}{4}\cdot \frac{(1{,}0\; M)^2}{0{,}5\; M }=0{,}5\; M](https://media.studieportalen.dk/images/equations/_9khM8w-BB6BttgS-KsdjA==.gif)