Kemi
opløsning regne opgave
Bestem massen (i gram) af den mængde Cl-ioner, der kan holde en opløsning med 10 mmol Mg²? elektrisk neutral.
Ifølge facit skal det give 0,709 g men det kan jeg ikke få :/
Svar #1
04. juli 2015 af Toonwire
Hejsa
Det første du skal indse er, at en reaktion mellem 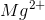 og
og 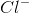 sker i forholdet 1:2 således, at molekylet bliver elektrisk neutralt. Der skal 2 negative ladninger fra chlor-atomet til at opveje magnesiums dobbelt positive ladning.
sker i forholdet 1:2 således, at molekylet bliver elektrisk neutralt. Der skal 2 negative ladninger fra chlor-atomet til at opveje magnesiums dobbelt positive ladning.
Dvs.
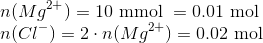
Så skal du bare slå molarmassen for Chlor op i en databog eller det periodiske system.
Benyt formlen
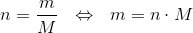
Prøv om du kan få det til det rette facit nu :)
Skriv et svar til: opløsning regne opgave
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.



