Kemi
Permanganat til mangan(II)
Hej
Jeg forsøger at lære at afstemme redoxreaktionsligninger. Jeg kigger på et eksempel, som viser at:
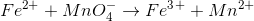
Jeg kan godt finde ud af at tildele OT, men jeg ved ikke, hvordan man opstiller disse i ligningsfunktionen herinde. Der står så i eksemplet, at når permanganat bliver til mangan(II), så går den 5 ned, og dette kan jeg slet ikke se - jeg ser, at den går 3 op. Kan nogen forklare dette?
Mvh. Emil
Svar #1
20. juli 2015 af Flamboyanten (Slettet)
Skriv et svar til: Permanganat til mangan(II)
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.


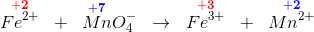
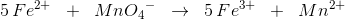
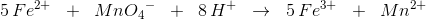
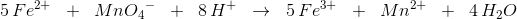
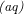 undtagen
undtagen