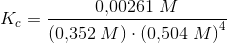Kemi
kemisk ligevægt
hej folkens
Jeg har denne opgave for i kemiopgaver. en kemi A bog:
3.1
Vi ser på reaktionen Fe^3+(aq)+4Cl^-(aq) --> FeCl_4^-
a) Opskriv reaktionsbrøken for reationen
(eventuelt et svar med en forklaring på hvordan det skal gøres)
I en vandlig opløsning eksistere ligevægten:
Fe^3+(aq)+4Cl^-(aq)<-->FeCl_4^-
Ved given temperatue findes følgende aktuelle koncentrationer af de tre ioner i ligevægt i opløsningen:
[Fe^3+] = 0,352M
[Cl^-] = 0,504 M
[FeCl_4^-] = 0,00261 M
b) beregn en værdi for ligevægts konstanten ved den pågældende temperatur
c) Vi koncentrationen af FeCl_4^- blive større eller mindre hvis der sættes salt-syre i opløsningen?
Skriv et svar til: kemisk ligevægt
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.








![\frac{\left [ Fe{Cl_4}^- \right ]}{\left [ Fe^{3+} \right ]\cdot \left [ Cl^- \right ]^4}](https://media.studieportalen.dk/images/equations/EkqU8shLH8hSjhZLV1PpIw==.gif)