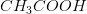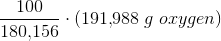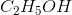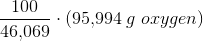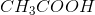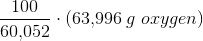Kemi
Mængdeberegniner
Hej, jeg har et problem med følgende spørgsmål:
B. Hvor meget oxygen skal der bruges til omsætning af 100g af hver af de 3 stoffer?
C. Hvor meget glucose, ethanol og eddikesyre kan man omsætte med 100g oxygen?
De følgende 3 stoffer, som der er tale om er glucose, ethanol og eddikesyre, som jeg allerede har afstemt. Så det ville være dejligt hvis der var nogen der kunne hjælpe mig med opgave B og C. På forhånd tak
Svar #1
08. oktober 2015 af mathon
Molforholdet er forholdet mellem de afstemte reaktionskoefficienter.
Dette forhold omregnes til masseforhold.
Svar #4
09. oktober 2015 af biotek222 (Slettet)
Men for at bruge formlen m=n*M, så er jeg vel nødt til at finde n ved den forrige formel n=m/M, ikke?
Svar #5
09. oktober 2015 af mathon
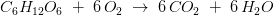
ækvivalente stofmængder: 1 mol 6 mol
ækvivalente masser n·M: 180,156 g 191,988 g
Svar #6
09. oktober 2015 af mathon
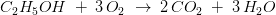
ækvivalente stofmængder: 1 mol 3 mol
ækvivalente masser n·M: 46,069 g 95,994 g
Svar #7
09. oktober 2015 af mathon
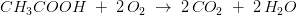
ækvivalente stofmængder: 1 mol 2 mol
ækvivalente masser n·M: 60,052 g 63,996 g
Svar #8
09. oktober 2015 af biotek222 (Slettet)
Så det vil altså sige, at:
C6H12O6: 180, 6O2: 1152, 6CO2: 1584,36, 6H2O: 648,576
CH3CH2OH: 46,07, 3O2: 288, 2CO2: 152,02, 3H2O162,15
CH3COOH: 60,05, 2O2: 64, CO2: 88,02, H2O: 36,04
Svar #10
09. oktober 2015 af biotek222 (Slettet)
Når på den måde.. Og så når der bliver spurgt om ved hvilken reaktion der dannes mest H2O og CO2, så er det vel bare med at erstatte oxygenen med H2O/CO2, ikke?
Skriv et svar til: Mængdeberegniner
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.


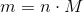 (som jo er den samme formel)
(som jo er den samme formel)