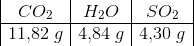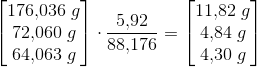Kemi
Mængdeberegning
I kemi (A-niveu) i 1.g på HTX, har vi fået en aflevering om mængdeberegning. Spørgsmålet lyder følgende:
Vi ser på reaktionen:
C4H8S (l) + O2 (g) → CO2 (g) + H2O (l) + SO2 (g)
Der anvendes 5,92 g C4H8S. Beregn masserne af produkterne i reaktionen.
Det som jeg vil spørge om:
1. Er produkterne det, der står på den højre side af pilen, altså CO2 (g) + H2O (l) + SO2 (g)? (Det er sådan jeg har forstået det.)
2. Massen er m og m = M × n. Når jeg får oplyst at vi har 5,92 g af C4H8S, er det så stofmængden (n) eller massen (m), som jeg får oplyst?
3. Hvordan bruger jeg den oplyste information til at finde masserne af de resterende "produkter"?
På billedet kan man se dét, som jeg indtil videre har præsteret at skrive ned i mit word-dokument.
Svar #1
17. februar 2016 af mathon
1.
Produkterne er stofferne på højre side af pilen,
men du har ikke afstemt reaktionen:
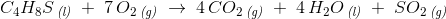
ækvivalente mængder 1 mol 4 mol 4 mol 1 mol
Svar #2
17. februar 2016 af mathon
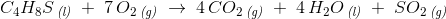
ækvivalente mængder 1 mol 4 mol 4 mol 1 mol
88,176 g 176,036 g 72,060 g 64,063 g
5,92 g x y z
resten er forholdsregning.
Svar #3
17. februar 2016 af Era
Med hensyn til molarmasse og stofmængde , har jeg så forstået følgende rigtigt?
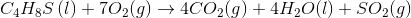
Stofmængde:
1mol 7mol 4mol 4mol 1mol
Molarmasse:
88,176 g 223,986 g 176,036 g 72,060 g 64,063 g
Masse:
5,92 g x y z
1 mol = 5,92 g
x = 4 mol
4 mol = 5,92 g * 4 = 23,68 g
x = 23,68 g
M(4CO2) = 23,68 g
y = 4 mol
4 mol = 5.92 g * 4
M(4H2O) = 23,68 g
z = 5,92 g
M(SO2) = 5,92 g
Er dette rigtigt forstået ( - og ikke mindst regnet)?
Skriv et svar til: Mængdeberegning
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.