Kemi
Mængdeberegning
Hej med jer. Håber i kan hjælpe mig. Er gået helt i stå ved dette spørgsmål..
Ved standardbetingelser ( 20 grader, 1 atm lufttryk) fylder 1 mol gas 24,1 L
- Hvor mange liter brint dannes der ved reaktionen?
Svar #1
30. april 2016 af Heptan
Du ved at gassen fylder 24,1 L/mol. Hvis du kender stofmængden af brint skal du bare gange det med det molare rumfang Vm.
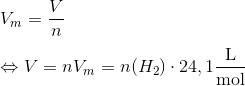
Svar #2
30. april 2016 af densødepigee (Slettet)
men hvordan finder jeg stofmængden af brint.. Det er nemlig kun disse oplysninger vi får?
Skriv et svar til: Mængdeberegning
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.

