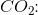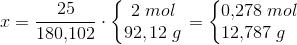Kemi
Teoretisk stofmængde for CO2 og maksimal masse af CO2
04. maj 2016 af
tobias249 (Slettet)
-
Niveau: B-niveau
Hej studieportalen.
Jeg undrede mig over hvordan jeg skal udregne den Teoretiske stofmængde for CO2, og derefter maksimal masse af CO2.
Reaktionen ser således ud:
C6H12O6 -> CO2 + 2CH3CH2OH
Derudover har jeg udregnet følgende:
Stofmængde af CO2: 0,2251 mol
Ethanol dannet i gram 10,3635
volume af ethanol: 0,13876 mol
Tak på forhånd.
Svar #2
04. maj 2016 af tobias249 (Slettet)
Mange tak. Ved du hvordan man udregner den teoretiske stofmængde og maksimal masse? :-)
Skriv et svar til: Teoretisk stofmængde for CO2 og maksimal masse af CO2
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.







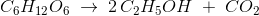
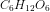 -mængden.
-mængden.