Fysik
Gay Lussacs love
22. juni 2016 af
Koplop (Slettet)
-
Niveau: B-niveau
Er der nogle der hurtigt kan forklare mig Charles' og Gay Lussacs love?
Tak!
Svar #1
22. juni 2016 af mathon
Charles lov, siger at trykket for en indespærret ideal gas med konstant volumen er ligefrem proportionalt med den absolutte temperatur.
Gay-Lussac's lov: Alle ideale gasser har ved konstant tryk - målt ud fra rumfanget ved 0°C - en rumudvidelseskoefficient på 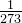 grad-1.
grad-1.
Skriv et svar til: Gay Lussacs love
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.







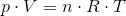
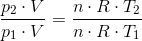
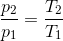
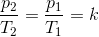
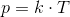 Charles Lov
Charles Lov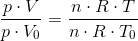
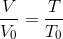
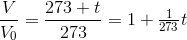
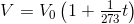 Gay-Lussac's lov
Gay-Lussac's lov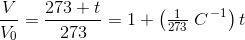
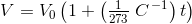 Gay-Lussac's lov
Gay-Lussac's lov