Kemi
relativ atomisk masse
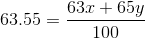
Kobber har to isotoper kobber-63 og kobber-65. Givet relativ atomisk masse, hvordan finder man procenterne af isotoperne?
Svar #1
28. august 2016 af Eksperimentalfysikeren
Du har to ligninger med to ubekendte.... Jo, den er god nok. Den ene står som formel i dit indlæg, den anden beskriver siger, at den samlede mængde er 100%, altså x+y=100.
Svar #2
28. august 2016 af hej908
ja men hvordan løser man en ligning med to ubekendte?
kan det være 50% = x og y
Svar #3
28. august 2016 af Eksperimentalfysikeren
Nej, Der er flere metoder. Den jeg vil fforeslå her er at du isolerer y i den sidste ligning; y=100-x. Det indsætter ud for y i den ligning, du har i forvejen. Så har du en enkelt ligning i x. Den løser du.
Pointen i opgaven er, at der tilsyneladend kun er én ligning med to ubekendte, men der er den skjulte ligning y+x=100, som udtrykker, at summen af mængderne af isotoperne er lig med den totale mængde, så der er to ligninger.
Svar #5
28. august 2016 af Eksperimentalfysikeren
Du har
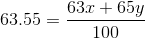
og
x+y = 100
Isoler y:
y = 100 - x
Indsæt i den første ligning:
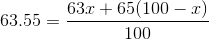
Løs ligningen.
Svar #7
28. august 2016 af Eksperimentalfysikeren
Gang på begge sider af lighedstegnet med 100. Så slipper du af med brøken.
Gang 65 ind i parentesen. Læg 2x tilpå begge sider af lighedstegnet og træk 63,55 *100 fra på begge sider af lighedstegnet. Divider til sidst med 2 på begge sider af lighedstegnet, så har du x.
Skriv et svar til: relativ atomisk masse
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.





