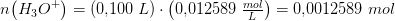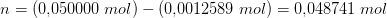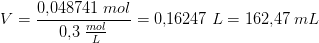Kemi
Titrering - udregne volume
19. oktober 2016 af
Jenskristiann
-
Niveau: A-niveau
" I et bægerglas skal titreres 100 ml 0,500 M HCl med en 0,300 M NaOH opløsning.
Hvor meget NaOH opløsning er der tilsat når pH er 1,90?" - lyder spørgsmålet.
Jeg har for det første fundet stofmængden af HCl, som lyder 0,500 M * 0,1 L = 0,05 mol.
Jeg tænkte på at bruge noget med pH = pKs+log(nb/ns), men jeg kan ikke rigtig regne mig frem til noget brugbart. Er der nogen, der sidder inde med nogle hints?
Tak på forhånd.
Skriv et svar til: Titrering - udregne volume
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.








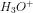 indeholder 0,05 mol
indeholder 0,05 mol 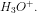
![\left [H_3O^+ \right ]=10^{-pH}\; M=10^{-1{,}90}\; M=0{,}012589\; M](https://media.studieportalen.dk/images/equations/hSAS97MMUBY-1_cmuNCpXw==.gif)