Kemi
plan
Hej er der nogle, som kan forklare mig, hvad der menes med den sidste del af opgaven, som understreget med grøn?
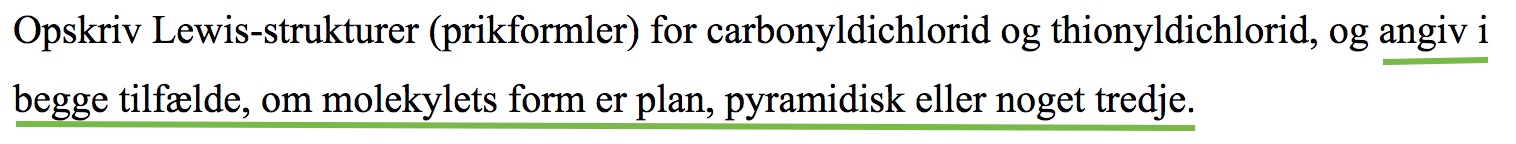
Svar #1
10. december 2016 af Toonwire
Du skal have fat i noget der hedder VSEPR-teori.
Hvis du har skrevet Lewis-strukturene op for molekylerne er det en smal sag, du skal bare kende navnet.
Lad os først kigge på carbonyldichlorid, 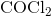
For dette molekyle binder Oxygen og to Chlor atomer sig til et Carbon atom.
Carbon har 4 elektroner i yderste skal og kan lave 4 bindinger:
- 2 af elektronerne bruges til at binde med hvert af chloratomerne
- de sidste 2 elektroner bruges til at indgå en dobbeltbinding med oxygenatomet.
Generelt kan molekylets opbygning skrives som 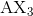
Hvor 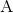 er center-atomet og
er center-atomet og 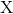 er de omliggende atomer, bundet til center-molekylet (se herunder):
er de omliggende atomer, bundet til center-molekylet (se herunder):


Sidenote: bindingsvinklen er ikke helt 120 pga. dobbeltbindingen "fylder" lidt mere
pga. dobbeltbindingen "fylder" lidt mere
Denne struktur kaldes planar - plan, idet du kan forestille dig at den kunne ligge fladt på et bord.
Udover dette er formen også trigonal - formet som en trekant.
Den samlede form for molekylet kaldes altså for planar, trigonal.

Det næste molekyle, thionyldichlorid 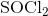 , er lidt sjovere i dens form.
, er lidt sjovere i dens form.


Igen, dobbeltbindingen skubber chloratomerne lidt tættere sammen
Svovl har 6 elektroner i yderste skal men deler kun 4 af disse elektroner (2 enkeltbindinger og 1 dobbeltbinding).
Det efterlader et frit elektronpar. Disse frie elektronpar fylder endnu mere og skubber så kraftigt til resten af bindingerne, at det der ville have været en plan struktur (trigonal planar som før) ikke længere kan ligge fladt:

Forestil dig at molekylet nærmest står på 3 ben, ligesom et kamerastativ.
Denne form på molekylet kaldes, meget nærtliggende, for pyramide.
Helt officielt hedder formen trigonal pyramidal (trekantet pyramide)
Svar #2
13. december 2016 af Sneharusha (Slettet)
ved du om der er et program der kan lave disse strukturer?

Skriv et svar til: plan
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.







