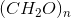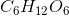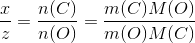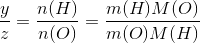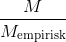Kemi
Empirisk formel
18. februar 2017 af
Bla99i (Slettet)
-
Niveau: B-niveau
Glucose, CxHyOz, indeholder 40,00 % C og 6,71 % H. Bestem glucoses empiriske formel, ogdernæst glucoses molekylformel, hvis molarmassen er 180,16 g/mol.
Kan ikke lige gennemskue hvordan jeg laver den...
Skriv et svar til: Empirisk formel
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.