Kemi
Kobber i zink og NaOH
Jeg er igang med at skrive raport til et forsøg jeg lavede forleden, men synes ikke at det giver mening.
Formålet med forsøget er følgende: Formålet med forsøget er at omdanne udseendet på en kobbermønt til sølv, og derefter gøre den guldfarvet.
teorien bag er: Når mønten nedsænkes i zinkat-ionerne begynder zinken at danne en hinde på ydersiden af kobbermønten, når man derefter opvarmer Zn(S) og Cu(s) blandes de to stoffer sammen på ydersiden af mønten, og får den til at se guldagtig ud.
men hvad der ikke giver mening er at mønten falder i vægt når den redoxere med zink og stiger igen når den opvarmes. nogle der har en ide om hvad der foregår ?
Skriv et svar til: Kobber i zink og NaOH
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.




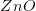 og
og