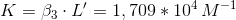Kemi
Ligevægtskonstant
Hej
Jeg sidder med vedhæftede opgave. Mit løsningsforslag var, at lægge følgende reaktionsligninger sammen:
PbSO4 --> Pb2+ + SO42-
Pb2+ + 3HO- --> [Pb(OH)3]-
_______________________
PbSO4 + 3OH- --> [Pb(OH)3]- + SO42-
Og benytte at der i opgaven er oplyst at: β3 = 1012,15 M-3 = [(Pb(OH)3)-]/[Pb2+]*[OH-]3
og L' = 1,21*10-8 M2 = [Pb2+]*[SO42-]
Men da ligevægten jeg ønsker at finde må være: K=[(Pb(OH)3)-]*[SO42-]/[PbSO4]*[OH-]3 kan jeg ikke se hvordan disse informationer kan lede til en værdi for k... da koncentrationen af PbSO4 ikke indgår i nogle af disse og jeg ikke skal bruge koncentrationen af Pb2+ som netop angives i form af opløselighedsproduktet. Håber nogen kan hjælpe.
PFT
Svar #2
17. marts 2017 af seltzer
Skriv et svar til: Ligevægtskonstant
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.