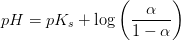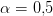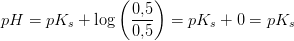Kemi
Aflæsning af pKs-værdi på titrerkurve
19. marts 2017 af
Heylisa
-
Niveau: B-niveau
Hvis man har en titrerkurve for en svag syre, hvorfor er det så at man kan aflæse pKs-værdien som pH-værdien halvejs mod ækvivalenspunktet?
Tak på forhånd :)
Svar #1
19. marts 2017 af janhaa
fordi weak acid, HA:
HA + H2O <=> H^+ + A^-
og ved half eq point is [HA] = [A^-] og
pH = pKs - log([HA]/[A^-]) = pKs
der log(1) = 0
Skriv et svar til: Aflæsning af pKs-værdi på titrerkurve
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.


 ,
,