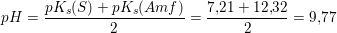Kemi
PH
19. maj 2017 af
Unintended96 (Slettet)
-
Niveau: Universitet/Videregående
Jeg sidder med denne her opgave, men kan ikke få det rigtige svar.
Hvad er pH i en 1,00 M vandig opløsning af Na2HPO4?
For H3PO4, gælder at:
Ka1 = 7.5*10^-3
?Ka2 = 6.2*10^-8
Ka3 = 4.8*10^-13
?svaret er 9.67, mit bud på opgaven er vedhæftet
Vedhæftet fil: Ph opgave.PNG
Skriv et svar til: PH
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.