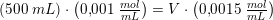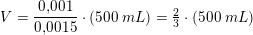Kemi
En lille opgave Hjælp
Hej
Er der nogen der kan løse og forklare denne opgave til mig, jeg får hele tiden et forkert svar.
Opgaven:
Fremstil 500 mL 1,0 HCl. Hvor mange mL 1,5 HCl skal der afmåles ?
Facit = 330
Svar #2
12. juli 2017 af ChemistryIsKey
Du skal tænke i retningen af fortyndingsloven.
Fortyndingsloven siger, at den stofmænde (i mol) du har før og efter fortyndingen af HCl SKAL være den samme, altså:
nfør = nefter
Loven stammer fra det faktum, at stof ikke kan opstå og forsvinde, men derimod er bevaret. Du ved formentlig, at stofmængden kan skrives som;
n = c · V
Altså stofmængden n findes ved at gange koncentrationen c og voluminet V sammen. Vha. dette kan du omskrive fortyndingsloven til;
cfør · Vfør = cefter · Vefter
Du starter med en opløsning på 1.5 M HCl og skal fremstille 500 mL 1.0 M HCl ud fra din startopløsning ved forytynding med vand.
Ud fra disse informationer har du altså følgende;
cfør = 1.5 M
cefter = 1.0 M
Vefter = 500 mL
Vha. fortyndingsloven kan du nu isolere Vfør (hvilket de spørger efter i opgaven) og du får;
Vfør = (cefter · Vefter) / cfør = (1.0 M · 500 mL) / 1.5 M = 333 mL
Din lærer/lærebog har formentlig afrundet resultatet, så de approksimere 333 mL til 330 mL (og det er jo kun 3 mL fra, så det går!).
Ud fra dine beregninger ved du nu, at for at fremstille 500 mL 1.0 M HCl, skal du anvende 333 mL (eller 330 mL) 1.5 M HCl og fortynde med vand op til 500 mL mærket.
Håber det hjælper lidt :)
Skriv et svar til: En lille opgave Hjælp
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.