Kemi
nogen der kan hjælpe
Hej...
Er der nogen der kan hjælpe, er virkelig kørt fast :(
Forklar hvordan man i et reaktionsskema angiver om et stof er et fast stof, en væske, på gas form eller om et stof er opløst i vand.
Svar #1
18. august 2017 af mathon
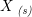 fast form s: solid
fast form s: solid
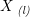 væskeform l: liquor = væske
væskeform l: liquor = væske
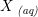 opløst i vand aq = aqua = vand
opløst i vand aq = aqua = vand
Svar #4
18. august 2017 af tøsenkolding (Slettet)
Super, det skriver jeg :) Tusind tak for hjælpen :)
Svar #5
18. august 2017 af tøsenkolding (Slettet)
3. Udpeg ved at indsætte tekstfelter på nedenfor stående Periodiske Systen følgende: Hovedgrupper, undergrupper, perioder. Og forklar hvad stoffer i samme hovedgruppe har til fælles. Og forklar hvad stoffer i samme periode har til fælles.
Svar #6
18. august 2017 af tøsenkolding (Slettet)
er det fint bare og skrive sådan ???
Det periodiske system er en tabel over alle kendte grundstoffer. Hovedgrupperne er de lodrette rækker og der er 8 hovedgrupper. Nummeret på hovedgruppen fortæller hvor mange elektroner der er i den yderste elektronskal. Undergrupperne i den samme hovedgruppe har fælles kemiske egenskaber. Perioderne er de vandrette rækker. Der er 7 perioder og nummeret på perioden er antallet af elektronskaller.
Svar #7
18. august 2017 af mathon
Stoffer, der befinder sig i en rækkefølge, hvor enten yderste s-orbital eller yderste p-orbital er under opfyldning samtidig med at alle d-orbitaler eller f-orbitaler indenfor enten ikke er påbegyndt eller helt opfyldte, kaldes hovedgruppestoffer. Alle andre grundstoffer har konstante s-orbitaler og p-orbitaler medens d-orbitaler og f-orbitaler varierer (er under opfyldning) og kaldes undergruppestoffer. Undergruppestofferne har principielt altid 2 s-elektroner i yderste skal, idet man dog finder eksempler på, at en s-orbital afgiver 1 eller 2 elektronmer til den nærmerste, indre d-orbital (se numrene 24, 29, 41, 42, 43, 44, 45, 46, 47, 77,78 og 79).
Det har vist sig, at stoffer med ens opbygning i yderste elektronskal har fælles kemiske egenskaber. De kemiske egenskaber afhænger for hovedgruppestoffernes vedkommende næsten udelukkende af elektronsystemet i yderste skal. De stoffer, der knyttes sammen på grund af ensartethed i elektron-opbygningen, er også snævert knyttet sammen gennem deres kemiske egenskaber.
Undergruppestoffer har principielt yderste s-orbital opfyldt, selvom det hyppigt ses, at én eller begge s-elektroner "hopper" ind til den indenfor liggende skals d-orbital, der er under opfyldning. Ofte vil undergruppestoffer have oxidationstrin, der er højere end deres gruppenummer. De må altså kunne afgive flere elektroner, end de har i yderste skal (højst 2). Dette betyder, at undergruppestoffernes valenselektroner kan findes blandt de to yderste niveauers elektroner.
Årsagen hertil er, at elektronernes energiforhold i disse stoffer hyppigt er temmelig ens i yderste skals s-orbital og i næstyderste skals d-orbital. Dette kan forklare, at der ved undergruppestofferne ofte optræder stærkt farvede ioner, der er paramagnetiske, let skifter oxidationstrin og viser stor tendens til kompleksdannelse, idet elektroner uden større hindring kan skifte fra den ene orbital til den anden selvom disse orbitaler tilhører forskelligt niveau.
Hovedgruppestofferne danner som hovedregel diamagnetiske forbindelser, der er farveløse.
Alle undergruppestofferne er ægte metaller. De danner positive ioner, men kan grundet deres store evne til kompleksdannelse, danne centralatom i komplekse syrerester. Dette er især i de højeste oxidationstrin.
Skriv et svar til: nogen der kan hjælpe
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.