Kemi
methan
find dernæst vha. Mængedeberegning, hvor meget massen af alle de indgående stoffer er, hvis der afbrandes 80,80 g methan.
__ CH4(g) + _ O2(g) à _CO2 (g) + _H2O (l)
Svar #1
18. september 2017 af janhaa
CH4 + 2O2 => CO2 + 2H2O
80,8 g CH4 => 5,05 mol CH4
32,3 g O2
222,2 g CO2
181,8 g water
Svar #2
18. september 2017 af mathon
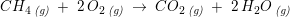
ækvivalente mængder: 1 mol 2 mol 1 mol 2 mol
16,043 g 63,996 g 44,009 g 36,030 g
aktuelle mængder 80,80 g x y z
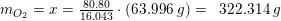
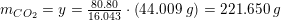
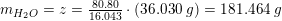
Svar #3
18. september 2017 af tøsenkolding (Slettet)
jeps havde fanget den _ :) .. Og når man så skal finde stofmængde i mol for de forskellige f,eks
n = 80,80 * 16,042 = ???
Svar #4
18. september 2017 af tøsenkolding (Slettet)
..
Hvad er massen af reaktanterne? ___________________g_
Hvad er massen af produkterne? ____________________g__
Forklar sammenhængen mellem massen af reaktanter og massen af produkter:
har fundet ud af reaktanterne og produkterne skal være en.. eller ?
Svar #5
18. september 2017 af tøsenkolding (Slettet)
kan det passe massen på begge er 4 ???
En reaktant er de substrater som bruges til at lave en kemisk reaktion.
Produkt
Når man f.eks har blandet nogle stoffer, så får man et produkt.
Svar #8
20. september 2017 af tøsenkolding (Slettet)
Hva så med denne hvis der står.
find dernæst vha.mængdeberegning, hvor meget massen af de andre stoffer er, for at der er ækvivalente mængder.
Ch3CH2OH(ag) + O2(g) ---> O2(g) + H2O
masse (g) 12
molarmassen (g/mol)
stofmængde(mol)
molforhold/koefficienten
Skriv et svar til: methan
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.