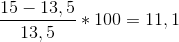Kemi
Destillation af rødvin
Hej. Jeg har lavet et forsøg med destillation af rødvin
Efterbehandling:
Vol-% på vinflaske: 13,5 %
Først skulle jeg beregne massen af ethanol-vand blandingen: 86,89 g (kolbe med indhold) - 38,93 g (kolbe uden indhold) = 47,96 g
Beregn densitenten af blandingen: Densitet = masse / volumen: 47,96 g / 50 mL = 0,9525 mLFind vol-% for ethanol-vand i blandingen: 30 %
Men så skal jeg finde vol-% for de oprindelige 100 mL vin, og det er det jeg har brug for hjælp til..
Det er til min eksamen i morgen, så jeg håber virkelig på hjælp.
På forhånd tak
Svar #1
16. juni 2016 af umolich
Når du skriver kolbe med og uden indhold - er det så efter du har afdestilleret ethanol?
Svar #3
16. juni 2016 af studerendeyo (Slettet)
file:///C:/Users/Mille/Downloads/Ethanol%20densitet%20vol-%25.pdf
Vi har det her, som jeg har slået op i, for at finde vol-% af destillatet :-)
Svar #4
16. juni 2016 af umolich
Så jeg gætter på at du har udtaget 50 ml rødvin, afvejet det, destilleret ethanol af, afvejet igen, og massen af den ethanol der er dampet af er 47,96 g. Dvs. at der har været 47,96 g ethanol i vinen - så skal du ikke beregne densiteten, men du skal bruge ethanols densitet (0.789 g/ml) for at beregne hvor mange milliliter de 47,96 g svarer til, og derefter beregne vol% ved at dividere med de 50 ml. Så har du vol% for de 50 ml og den er naturligvis den samme som i de 100 ml.
Svar #5
16. juni 2016 af studerendeyo (Slettet)
Det er 100 mL vin som jeg har destilleret, og destillatet af ethanol-vand vejede 47,96 gram..
Svar #7
16. juni 2016 af studerendeyo (Slettet)
Øvelsesvejledningen ser sådan ud:
Svar #8
16. juni 2016 af umolich
Okay, nu er jeg med.
Du har dampet AL ethanol fra 100 ml vin over i en 50 ml kolbe, som du så har fyldt med vand, og beregnet densiteten og derefter ethanol vol% af. Hvis du får en vol% på 30% i 50 ml, og al den ethanol oprindeligt var i 100 ml - kan du så selv regne ud hvad vol% var i de 100 ml?
Skriv et svar til: Destillation af rødvin
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.