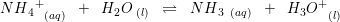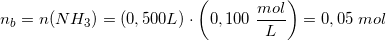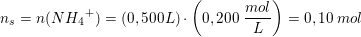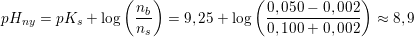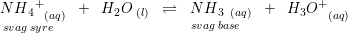Kemi
puffer
Hej, er der nogle gerne vil hjælpe mig med denne opgave? :) Jeg skal bruge mængdeberegning i den første (tror jeg), men ikke helt hvordan.

Svar #1
20. august 2014 af Heptan
Du skal bare bruge pufferligningen :-)

så indsæt ammoniums pKs, og de respektive koncentrationer
Svar #2
21. august 2014 af inddd (Slettet)
Tænkte på i b'eren så blandes NH4+ med HCl, men hvordan går det an når det to syrer? (eller er det bare mig som har misforstået opgaven?)
Skriv et svar til: puffer
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.