Kemi
Natriumhydroxid volumen
hej! Jeg er tvivl om følgende opgave:
Beregn volumenet af den portion natriumhydroxid, der skal anvendes til fremstilling af pufferopløsningen.
Har søgt lidt rundt omkring, men har ikke helt kunne finde ud af det. jeg ved jeg skal bruge pufferligningen til et eller andet.
Vil i være venligst at forklare mig trin for trin, så jeg kan følge med? :D I behøver ikke give mig resultatet :D
tak på forhånd :D
Svar #1
21. oktober 2014 af Heptan
Det er også lidt svært at give dig resultatet når du ikke har givet os nogle tal eller opløsninger ;)
Men ja, du skal bruge pufferligningen, formentlig også c = n/V, måske n = m/M og ellers bare sund fornuft. Måske også et reaktionsskema vil hjælpe
Svar #2
21. oktober 2014 af erinaa (Slettet)
#1Det er også lidt svært at give dig resultatet når du ikke har givet os nogle tal eller opløsninger ;)
Men ja, du skal bruge pufferligningen, formentlig også c = n/V, måske n = m/M og ellers bare sund fornuft. Måske også et reaktionsskema vil hjælpe
hehe ja, det kan jeg godt se!
men hvordan skal jeg bruge pufferligningen?
jeg har en pufferopløsning med en pH værdi på 4,5. den fremstilles ved at blande 100 mL 0,075 M tropinsyreopløsning med en portion 0,1 M natriumhydroxid.
Svar #3
21. oktober 2014 af Heptan
Du skal finde ud af hvad pKs for tropinsyre er.
For at løse opgaven skal du "regne baglæns", og gøre således:
For at finde ud af hvor stort et volumen NaOH der skal anvendes, skal du finde ud af hvor stor en stofmængde der skal bruges.
Man kan ofte antage at stofmængden af NaOH der forbruges er identisk med stofmængden af svag syre der omdannes ved reaktionen:
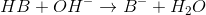
Man antager altså, at reaktionen ikke forløber mod venstre. Desuden ser man bort fra vands egendissociation.
Da syren er svag, kan vi endvidere antage at den ikke nævneværdigt dissocierer (man kan gøre prøve ved at beregne stofmængden ns og nb i svag syre opløsningen, og opdage at det ikke gør en væsentlig forskel), dvs. at ns (før) = ns (efter) (bemærk at jeg taler om svag syre opløsningen, og ikke pufferopløsningen)
Det antages altså at nb (efter) = n(OH-)før, og at ns (puffer) = ns (svag syre opløsning) - n(OH-)før
Heraf løses ligningen for n(OH-)før
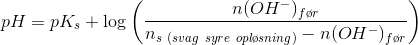
Jeg håber ikke mine mærkelige notationer forvirrer dig ... :)
Svar #4
21. oktober 2014 af erinaa (Slettet)
Jeg forstår hvad du skriver! Tusind tak for hjælpen! :D
Skriv et svar til: Natriumhydroxid volumen
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.







