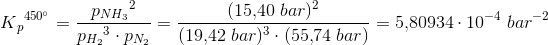Kemi
Ammoniakligevægten
Hej!
Jeg har brug for hjælp så hugtigt som muligt!
Tak på forhånd!
-----------------------------------------------------------------------------------------------
Betragt Ammoniakligevægten: 3H2(g) + N2 (g) <--- ---> 2NH2 (g).
I en ligevægtsblanding i en lukket beholder ved 450ºC måles følgende partialtryk for de tre gasser
p(NH3) = 1,763 bar
p(N2) = 6,675 bar
p(H2) = 21,87 bar
a) Beregn Kp ved 450ºC
b) Beregn det totale tryk i beholderen ved ligevægt.
c) Undersøg, om nedenstående blandinger ved 450º?C er nået til ligevægt. Hvis ikke, angiv da nettoreaktinens retning, når ligevægten indstiller sig.
p(NH3) = 15,40 bar = 325,9 bar
p(N2) = 19,42 bar = 55,74 bar
p(H2) = 65,99 bar = 210,8 bar
Svar #1
26. oktober 2015 af GalVidenskabsmand (Slettet)
a)
Kp = p(NH3)2/( p(N2) * p(H2)3 )
b)
ptotal = p(NH3) + p(N2) + p(H2)
c)
I hvert tilfælde beregn brøken
p(NH3)2/( p(N2) * p(H2)3 )
Hvis brøken er lig Kp fra spørgsmål a), er der ligevægt. Hvis brøken er mindre end Kp, vil nettoreaktionen forløbe mod højre på vej mod ligevægt (for at gøre tælleren større og nævneren mindre). Hvis brøken er større end Kp, vil nettoreaktionen forløbe mod venstre på vej mod ligevægt ( for at gøre tælleren mindre og nævneren større).
Skriv et svar til: Ammoniakligevægten
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.


 2 NH
2 NH