Kemi
Syrestyrke
Nogle som kan hjælpe mig med denne opgave:
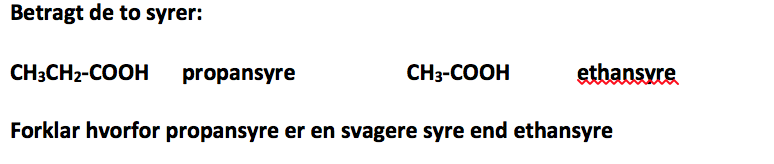
Svar #1
29. oktober 2015 af mathon
En 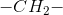 gruppes elektronaffinitet er ikke særlig stor,
gruppes elektronaffinitet er ikke særlig stor,
hvorfor syrestyrkeforskellen mellem ethansyre og propansyre ikke er ret stor:
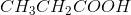
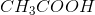
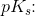
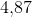
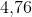
Svar #2
29. oktober 2015 af serieaddicted
Det afhænger af hvor mange kulstof atomer syren indeholder. Jo færre c-atomer, jo stærkere en syre.
Svar #4
29. oktober 2015 af serieaddicted
Må nok hellere ændre min forklaring for det er ikke alle syrer der indeholder c-atomer. Syre er defineret som et molekyle eller en ion, der kan afgive en hydron (H+). Grunden til at propansyre er en svagere syre end ethansyre er, at propansyre ikke afgiver alle H+ ionerne ved reaktion med vand, mens ethansyre reagere fuldstændigt med vand.
Undskyd for forvirringen...
Håber denne forklaring var bedre.
Svar #5
29. oktober 2015 af Heptan
Ethansyre reagerer ikke fuldstændigt med vand, men dissocierer ca. 1 % afhængig af koncentrationen.
De to carboxylsyrer er sammenlignelige, men propansyre er en svagere syre, fordi alkylgrupper er elektrondonerende. Hvis der er flere elektroner omkring carboxylsyrecarbonatomet giver den ikke ligeså let slip på H+ som jo er en positiv ion.
Skriv et svar til: Syrestyrke
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.

