Kemi
Titrering
En stofprøve A, består af en blanding af natriumcarbonat, natriumhydrogencarbonat og kaliumchlorid.
0,500 g af denne blanding opløses i 50 mL demineraliseret vand.
Opløsningen titreres med 0,115 M HCl.
Ækvivalenspunkterne aflæses til hhv. 9.63 mL og 34.27 mL
Opgave)
Beregn den procentvise sammensætning i masseprocent af stofprøven A
Svar #2
28. november 2015 af mathon
n1(HCl) = (9,63 mL)*(0,115 mmol/mL) = 1,10745 mmol dvs 0,00110745 mol Na2CO3
n2(HCl) = ((34,27-9,63) mL )*(0,115 mmol/mL) = 2,8336 mmol dvs 0,0028336 mol NaHCO3
masser:
Na2CO3 NaHCO3 KCl
(0,00110745 mol)·(108,988 g/mol) (0,0028336 mol)·(84,0066 g/mol)
0,120699 g 0,238041 g 0,14126 g
%Na2CO3 %NaHCO3 %KCl
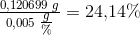
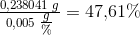
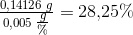
Svar #3
28. november 2015 af Kemifjols (Slettet)
Tak!!!
Det eneste spørgsmål er bare, hvor du får massen af KCl fra?
Skriv et svar til: Titrering
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.