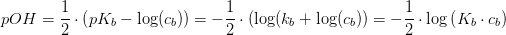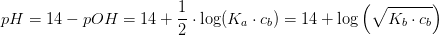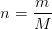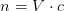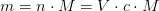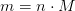Kemi
Mængde- og pH-beregning
Hej, har problemer med følgende opgaver:
1a. Beregn pH i 0,5M KOH
2a. Beregn koncentrationen af den opløsning, der fremkommer ved opløsning af 10 gram calciumhydroxid, Ca(OH)2, i en liter vand
3a. Beregn pH i opløsningen af Ca(OH)2 under antagelse af, at OH- er en stærk base
4a. NH3 er en svag base. Beregn pHi 2M ammoniakvand under antagelse af, at pKb for NH3 er 4,75
1b. Hvor mange mol HCl er der i 500ml 12M HCl-opløsning?
2b. Du skal fremstille en liter 3M opløsning af kobbersulfat – hvor mange gram kobbersulfat skal afvejes?
3b. En virksomhed har købt 2megamol (to millioner mol) natriumhydroxid. Hvor mange kilogram NaOH skal de finde plads til?
4ba. 100gram NaCl reageres med overskud af svovlsyre til gasformig HCl efter reaktionen NaCl + H2SO4 → HCl + NaHSO4. Hvor mange gram HCl dannes?
4.bb. Hvis alt den dannede HCl-gas opløses i en liter vand – hvad bliver så koncentrationen af den resulterede saltsyre?
Svar #2
19. oktober 2014 af mathon
2a.
Beregn antal opløste mol calciumhydroxid.
Beregn den molære koncentration af calciumhydroxid.
Svar #8
19. oktober 2014 af mathon
4ba.
Ud fra molforholdet beregnes antal mol NaCl.
Beregn den ækvivalente stofmængde HCl.
Omregn denne til gram.
Skriv et svar til: Mængde- og pH-beregning
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.









![\left [ OH^- \right ]=c_{KOH}=0,5\; M](https://media.studieportalen.dk/images/equations/-jw04vAuuok-HUg1oaWFPA==.gif)
![pH=14+\log\left (\left [ OH^- \right ] \right )=14+\log\left (0,5 \right )](https://media.studieportalen.dk/images/equations/M7d4KJrufhQ1wgbhvQIz3g==.gif)