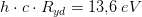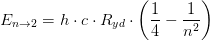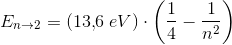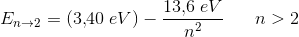Fysik
Atomfysik, Balmerserien
Forstår ikke helt denne her opgave, det ville være skønt hvis nogen kunne hjælpe :)
Har vedhæftet et billede af opgaven
Svar #3
12. oktober 2016 af iamanonymous
Har styr på alt undtagen sammenligningen. Er ikke helt sikker på, hvordan jeg sammenligner dem? :)
Svar #4
12. oktober 2016 af peter lind
Du mener formentlig forklaring af sammenhængen mellem energispringene og det viste spektrum. Du skal forklare hvilken overgange der svarer til de viste linjer.
Svar #5
12. oktober 2016 af iamanonymous
Kan det passe at n=2 svarer til det røde lys, n=3 svarer til lyseblå, n=4 til mørkeblå, n=5 og n=6 til de lilla?
Men jeg skal vel uddybe lidt mere
Svar #6
13. oktober 2016 af peter lind
Du skal altså angive hvorfra springet går og hvortil springet ender.
Skriv et svar til: Atomfysik, Balmerserien
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.