Kemi
Opløsning af Nacl
08. juni 2017 af
Sis23
-
Niveau: Universitet/Videregående
Hvorfor ikke nummer 3, ( 500 ml 1 M Nacl? )
250 ml 1M Nacl er også samme som 500 ml 1M, ikke?
Kan nogen forklare det overhovet hvordan denne løses?
250 ml 1M Nacl er også samme som 500 ml 1M, ikke?
Kan nogen forklare det overhovet hvordan denne løses?
Vedhæftet fil: IMG_0850.PNG
Svar #4
08. juni 2017 af Sis23
Undskyd, jeg menter hvorfor ikke nummer 4, ( 500 Ml 1M Naoh)? Det rigtig svar står der 3, men jeg tror 4 og 3 har samme reultat.
Skriv et svar til: Opløsning af Nacl
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.




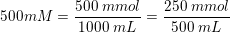
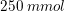 er indeholdt i
er indeholdt i 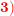
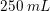
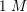
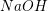 , som fortyndes til 500 mL opløsning.
, som fortyndes til 500 mL opløsning.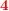 er forkert,
er forkert,