Matematik
Er dette korrekt? jeg er lidt i tvivl..
Ændring % = (vægt efter - vægt før) · 100)/(vægt før) %
0,0%: (6.5 g - 5,0 g)·100/(6,5 g )=23,07%
0,5%: (5,4 g – 4,3 g)·100/(5,4 g)=20,37%
1,0%: (5,6 g - 5,0g)·100/(5,6 g)=10,71%
3,0%: (3,2 g - 4,0 g)·100/(3,2 g)= - 25%
?Kan det passe at det giver -25%. Jeg er lidt forvirret nu..
Svar #1
01. oktober 2016 af VandalS
Du dividerer med det forkerte af tallene i alle delopgaverne, ellers ser det fint ud. Der er ikke noget galt i at få et negativt tal hvis der forsvinder masse, da du regner i forhold til den oprindelige vægt.
Svar #4
01. oktober 2016 af StoreNord
Jeg synes #0 ser helt rigtigt ud.
Ændringen skal selvfølgelig være i forhold til, hvad vægten var før.
Svar #5
01. oktober 2016 af Mm98
0,0%: (6.5 g - 5,0 g)·100/(5,0g )= 30%
Skal jeg så skrive 30% eller 0,3 % ? :)
Svar #6
01. oktober 2016 af Mm98
Umiddelbart vil jeg tro at jeg skal skrive 0,3% men jeg er ikke helt sikker. :)
Svar #8
01. oktober 2016 af StoreNord
0,3 % ville være forkert! Det er 30% også. 23,07% er det rigtige!
Svar #9
01. oktober 2016 af VandalS
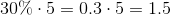 , som er forskellen mellem 6.5 og 5.
, som er forskellen mellem 6.5 og 5.
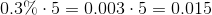 , som ikke har nogen direkte knytning til opgaven.
, som ikke har nogen direkte knytning til opgaven.
Svar #12
01. oktober 2016 af VandalS
#11 Vores forvirring opstår af at du i #0 bruger to forskellige talværdier for den samme variabel i din formel. Hvis du kan klargøre, hvilken af værdierne der er den rigtige kan vi blive enige om det rigtige resultat.
Svar #13
01. oktober 2016 af Mm98
Ændring % = (vægt efter - vægt før) · 100)/(vægt før) %
5,0 g - Før
6.5 g - Efter
Var det bedre:)) ?
Svar #14
01. oktober 2016 af VandalS
Så er svaret at ændringen er 30% i forhold til den originale vægt, da
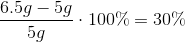 ,
,
som du kan tjekke ved at se om
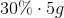 giver det samme som
giver det samme som 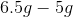
Svar #15
01. oktober 2016 af Mm98
Okay, mange tusind tak for hjælpen!!
Når jeg så er færdig med at beregne det, så skal jeg vel også skrive hvad jeg kan se osv. Hvad kan være grunden til at vi får et negativ tal i den sidste? Er det pga. massen eller hvordan?
Svar #16
01. oktober 2016 af VandalS
Din "vægt efter" er mindre end din "vægt før", så der er gået masse tabt. Ændringen i forhold til din originale masse er derfor negativ.
Svar #18
01. oktober 2016 af Eksperimentalfysikeren
Du har ikke angivet, hvad det er for et materiale, du regner på. Det kunne f.eks. et stykke træ. Det kan optage vand fra luften i fugtige perioder, og afgive vand i tørre perioder. I en fugtig periode vil træets masse stige, og så er ændringen positiv. i en tør periode vil massen falde og ændringen bliver negativ.
Svar #19
01. oktober 2016 af Mm98
Jeg har lavet et forsøg om osmose i kartofler, hvor vi vejede kartoflen før og efter vi lagde den ned i NaCl :)
Svar #20
02. oktober 2016 af AMelev
Har du vejet på forskellige tidspunkter - eller ved forskellige NaCl-koncentrationer. Du skriver bare før og efter, men du har 4 datasæt?
Osmose går jo ud på, at udligne kocentrationsforskelle. I dit tilfælde har du fokuseret på NaCl (uden for kartoflen). Det kan måske godt tænkes, at der er stoffer i kartoflen, som vil påvirke den modsatte vej.





