Kemi
Opgave med molekyleformel
Hejsa!
Jeg var syg den dag vi lavede den her opgave, og ved desværre ikke hvordan de er kommet frem til det de er.
Opgaven:
En ukendt organisk forbindelse A blev analyseret og man fandt at A indeholdt 8,80 g CO2 og 4,50 g H2O. Ydermere blev den molare masse bestemt til at være 74,12 g/mol.
Bestem molekyleformlen for A.
De andre har fået det til C4H10O, men jeg kan simpelthen ikke se hvordan?
Har fundet frem til :
nC=0,2mol
nH=0,5mol
Svar #1
26. august 2016 af mathon
Der er i opgaveteksten ikke nævnt noget om, hvilke grundstoffer 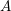 indeholder.
indeholder.
Ofte består analysen i en oprejning af forbrændingsprodukter dvs tilsætning af 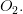
Herudfra kan indholdet af 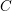 og
og 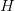 bestemmes til
bestemmes til
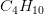 men mol massen af dette er under 74,12 g,
men mol massen af dette er under 74,12 g,
hvorfor molekylet er
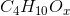 da det af analyseresultatet ikke fremgår, om molekylet
da det af analyseresultatet ikke fremgår, om molekylet
evt. også indeholder O-atom(er).
Skriv et svar til: Opgave med molekyleformel
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.






