Kemi
Vedrørende pH ...
1) Beskriv hvordan 0,1 M saltsyre kan fortyndes til 0,001 M saltsyre. Der skal
fremstilles 100 mL.
2) I samtlige forsøg i øvelse 1 må de målte pH-værdier ikke afvige med mere end 0,2
pH-enheder fra de beregnede værdier. Beregn hvor mange procent
koncentrationen på en opløsning af 0,0010 M saltsyre må afvige for at den netop
overholder kravet om maksimal afvigelse på 0,2 pH-enhed over den beregnede pH-værdi.
Vejledning: Du skal omregne pH-værdier til [H+]
Mangler der ikke flere oplysninge til sidst nævnte? Jeg håber på jeres hjælp.
Tak på forhånd!
Svar #1
24. september 2016 af mathon
1)
100 mL 0,001 M saltsyre er identisk
med
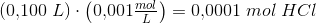
som skal skaffes fra et ukendt volumen 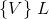 af
af 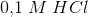
hvoraf:
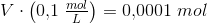
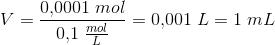
1 mL 0,1 M HCl fortyndes med 99 mL demineraliseret vand til frembringelse af 100 mL 0,001 M HCl.
Svar #2
24. september 2016 af sansas
Mange tak for hjælpen. Vedr. det andet spørgsmål mangler der ikke flere informationer? Jeg har jo ikke noget pKa værdi her? Eller skal det bruges overhovdet her...?
Svar #5
25. september 2016 af sansas
Hej,
Mange tak for hjælpen. Dog vil jeg spørge dig, hvilket formel du bruger her. Hvad hedder metoden, så jeg kan benytte den i fremtiden. Hvordan vil man så regne opgaven, når det andet sp. siger, at "kravet om maksimal afvigelse på 0,2 pH-enhed under den beregnede pH-værdi. " Det er samme formulering som det andet sp...
Håber på din hjælp.
Mange tak på forhånd.
Skriv et svar til: Vedrørende pH ...
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.










