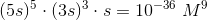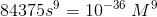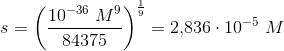Kemi
Hjælp til ligevægte opgave :(
Hej derude :)
Har brug for hjælp til en ligevægts opgave.... faktisk alle spørgsmålene :/
tak på forhånd :)
Svar #2
24. april 2015 af Heptan
a)
![K_0=[Ca^{2+}_{\ (aq)}]^5\cdot [PO_3^{3-}_{\ (aq)}]^3\cdot [OH^-_{\ (aq)}]](https://media.studieportalen.dk/images/equations/2r6xWtwEfv_rCRvO-0T_qw==.gif)
b)
Kaldes den molære opløselighed for s fås
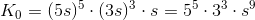
Løses ligningen fås
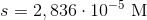
som kan omregnes til mg/L ved at gange med den molare masse for calciumhydroxidphosphat:
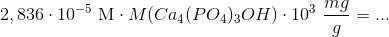
c)
Bliver miljøet mere surt øges koncentrationen af oxonium, og af ionproduktet
![K_v=[H_3O^+][OH^-]](https://media.studieportalen.dk/images/equations/o2n6oCEKZtJt1gik8lfNMQ==.gif)
kan vi se at koncentrationen af hydroxid må blive mindre som konsekvens heraf. Dvs. vi fjerner hydroxid, og derved forskydes ligevægten mod højre jf. Le Chateliers Princip, og opløseligheden øges.
For at modvirke dette indgreb, børster vi tænder flere gange om dagen med fluorholdig tandpasta, der skal udskifte hydroxid med fluorid (i hydroxyapatit), således at vores tænder bliver stærkere og ikke så let opløses i fx cola.
Skriv et svar til: Hjælp til ligevægte opgave :(
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.








![\left [Ca^{2+} \right ]^5\cdot \left [P{O_{4}}^{3-} \right ]^3\cdot \left [OH^{-} \right ]=10^{-36}\: M^9](https://media.studieportalen.dk/images/equations/KNadZyUywywA9j7xE1Fwuw==.gif)
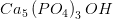 for
for