Kemi
Hjælp til 3 opgaver
Jeg har virkelig svært ved de 3 sidste spørgsmål i det dokument jeg vedhæfter. Det er opgave 3 spørgsmål 3,4,5. Der er svar fra de tidligere spørgsmål som skal bruges til at svare de 3 sidste spørgsmål med.
Håber der er nogen der gider at kigge på det og hjælpe mig videre...Jeg skal nemlig aflever det i dag.
Svar #2
20. oktober 2016 af HFNU (Slettet)
Ja det kan jeg godt se det har du ret i. Jeg oploader opgaven her igen
Svar #3
20. oktober 2016 af Skaljeglavedinelektier
3. Brug reaktionsforholdet og stofmængden af KMnO4 i ækvivalenspunktet.
4. Du har stofmængden fra opg. 3 og volumen.
5. Du har stofmængden og kan finde molarmassen.
Det ovenstående kræver selvfølgelig korrekte foregående opgaver - jeg har ikke tjekket om, de er lavet korrekt.
Svar #4
20. oktober 2016 af HFNU (Slettet)
Rigtig mange 1000 tak.
3. Jeg skal finde stofmængden af fe?2??+?, hvordan skulle jeg udefra det andet stof KMnO4? og ækvivalensforholdet finde stofmægden for fe?2+
4. Jeg ved stadig ikke hvordan jeg finder koncentrationen af Fe?2+ ?.....undskyld, jeg tror jeg har glemt hvordan man regner sådan noget ud.
5. Kigger jeg lige på igen...
Svar #5
20. oktober 2016 af Skaljeglavedinelektier
1) 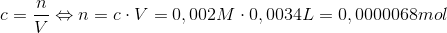
2) 1:5
3) Stofmængden af Fe2+ må være 5 gange større grundet reaktionsforholdet:
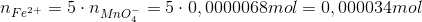
4) 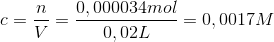
5) 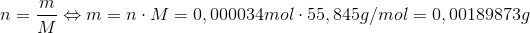
Svar #6
21. oktober 2016 af mathon
Bemærk:
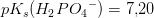
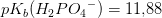 dvs betydeligt stærkere som syre
dvs betydeligt stærkere som syre
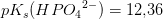
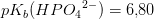 dvs betydeligt stærkere som base
dvs betydeligt stærkere som base
Svar #7
21. oktober 2016 af HFNU (Slettet)
Mange mange tak. Jeres hjælp betyder rigtig meget for mig. Tak.
Jeg har bare lige brug for at forstå pKs og pK?b helt rigtigt er det syrestyrken og basestyrkens konstant
Svar #8
21. oktober 2016 af Skaljeglavedinelektier
En base og en syres styrke angiver deres evne til at reagere med vand. Ved ligevægt er reaktionsbrøken lig med ligevægtskonstanten. Eksempel med ethansyre:
![\frac{[H_3O^+]\cdot [CH_3COO^-]}{[CH_3COOH]}=K_s](https://media.studieportalen.dk/images/equations/h4IHjigUEScLnqOvVIQK4w==.gif)
Ligevægtskonstanten Ks er ethansyres styrkekonstant. Jo støre styrkekonstant jo mere af syren er omdannet til den korresponderende base og oxoniumioner. pKs-værdier er bare en måde at få nogle lidt mere medgørelige/pæne værdier. Definition:
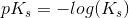
Styrken af syren defineres helt analog til basen. Styrkekonstanten kaldes bare for Kb.
Svar #9
22. oktober 2016 af mathon
#0
Bemærk sammenhængen:
Jo større 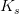 desto stærkere syre.
desto stærkere syre.
Jo mindre 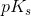 desto stærkere syre.
desto stærkere syre.
og tilsvarende for baser.
Svar #10
30. oktober 2016 af HFNU (Slettet)
Tak svar 9 mathon
Jeg har lige et spørgsmål til #5
spørgsmål 4; er det så de 20,00mL du dividerer med 1000 og får 0,02L
spørgsmål 5: Tallet 55,845 er det molarmassen
Svar #11
30. oktober 2016 af HFNU (Slettet)
Hvad kan man skrive i opgave 2 i det vedhæftede dokument ; Vi betragter titrering af phosphorsyre med natriumhydroxid. Se figur side 150. Kommenter antal mL natriumhydroxid der er brugt ved hvert ækvivalenspunkt.
Jeg har vedhæftet billede af grafen.
Jeg har skrevet det her: Jeg ved at det stiger med 5 mL NaOH for hver ækvivalenspunkt, men er der mon en grund til det? hvordan kan man kommenter grafen mere.
a) Ved 1.ækvivalenspunkt er der anvendt 5mL NaOH
b) Ved 2.ækvivalenspunkt er der anvendt 10mL NaOH
c) Ved 3.ækvivalenspunkt er der anvendt 15 ml NaOH
Skriv et svar til: Hjælp til 3 opgaver
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.


