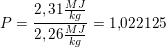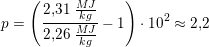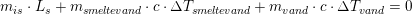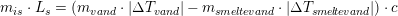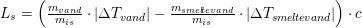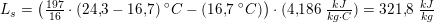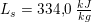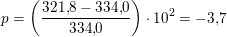Fysik
Hjælp til simpel procentafvigelse
Hej
Jeg har ved et forsøg fundet værdien for vands specifikke smeltevarme og fordampningsvarme også er min opgave at sammenligne værdien med tabelværdien, altså - Hvor mange procent er værdien for stor i forhold til tabelværdien?
Jeg er i tvivl om jeg beregner vands specifikke smeltevarme rigtigt og om procentafvigelsen under vands specifikke fodampningsvarme er rigtig.
Vands specifikke smeltevarme: 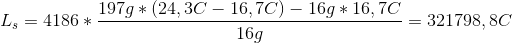
Vands specifikke fordampningsvarme: 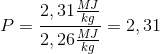 %.
%.
På forhånd tak.
Svar #1
03. august 2017 af hesch (Slettet)
Dit opgivne er temmelig uoverskueligt:
Du skriver at Ls er den specifikke fordampningsvarme, men opstiller et udtryk der har enheden [ºC]:
Udtrykket er således forkert, for den korrekte enhed skal være: [J/(kg * ºC )]. Du kan ikke blot rette enheden på højre side, for så stemmer den ikke med brøkens enheder.
Sådanne fysiske enheder har bl.a. til formål at kunne checke om et udtryk er korrekt. De skal stemme.
Hvad dækker disse temperatur- og masseangivelser over? Du må forklare forsøgsopstillingen.
Har disse 4186 at gøre med [ J/cal ] eller hvad?
Svar #2
03. august 2017 af annahansen2
#1 Jeg skal beregne vands specifikke fordampningsvarme. Der kan jeg gøre vha. formlen: ?
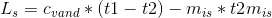
Cvand =4186 J/kg/ºC
mvand = 197g
mis = 16g
t1 = 24,3 ºC?
t2 = 16,7 ºC
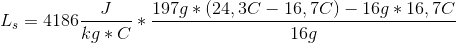
Nu er jeg bare i tvivl om det er rigtigt det som jeg gør. Derfor spurgte jeg herinde.
Svar #3
03. august 2017 af hesch (Slettet)
Jamen du er velkommen at spørge "herinde".
De 1486 [J/(kg*K)] er så vands varmekapacitet.
Du skal bestemme vands fordampningsvarme. Jeg har så skrevet forkert i #1, for enheden for denne fordampningsvarme er [J/kg].
Højrebrøken i dit udtryk har enheden [K], og multipliceret med varmefylden fås enheden [J/kg], der er korrekt.
Nu er det så, at med min indskrænkede forestillingsevne, ville jeg bestemme fordampningsvarmen ved - i en termisk isoleret opstilling - at tilføre kogende vand en kendt energimængde ( vha. dypkoger ), at veje dette vand før og efter denne energitilførsel, for til sidst at beregne forbrugt energi pr. kg fordampet vand.
Det er jo forholdsvist enkelt, men jeg fatter ikke hvordan denne is kommer ind i billedet? Du fordamper næppe vand ved 0ºC. Det bliver i hvert fald et langvarigt forsøg.
Sig mig, er det i virkeligheden vands smeltevarme opgaven handler om?
Der er lidt kludder/sammenblanding af de to begreber i de foranstående indlæg.
Svar #5
04. august 2017 af annahansen2
#3 Min fejl. Alt det jeg har skrevet i #2 er en opgave om smeltevarme.
Skriv et svar til: Hjælp til simpel procentafvigelse
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.