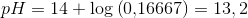Kemi
PH
14. april 2015 af
lalala1122 (Slettet)
-
Niveau: Universitet/Videregående
Der opløses 2 gram NaOH i 300 mL vand. Det kan antages, at volumen forbliver uændret. Hvad bliver pH af opløsningen?
Svar #2
14. april 2015 af lalala1122 (Slettet)
Det ser ikke helt rigtigt ud?
Vedhæftet fil:Skærmbillede 2015-04-14 kl. 18.06.07.png
Skriv et svar til: PH
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.


![pH=14+\log\left ( \left [ OH^- \right ] \right )](https://media.studieportalen.dk/images/equations/CRyVnu2_JVchyNBgK6uJtw==.gif)
![\left [ OH^- \right ]=c\left ( NaOH \right )=\frac{n}{V}=\frac{\frac{m}{M}}{V}=\frac{\frac{2\; g}{40,00\; \frac{g}{mol}}}{0,300\; L}=0{,}16667\; M](https://media.studieportalen.dk/images/equations/QaAp9efWlFSr2foyASUcOg==.gif)