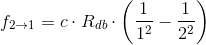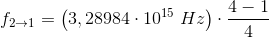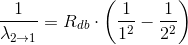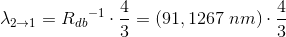Fysik
Regne frekvens for stråling på hydrogen.
Hej.
Jeg har siddet i omkring et kvarter med det samme spørgsmål om hydrogen, og opgaven lyder sådan her:
Forskellen i energi mellem de to laveste tilstande n=1 og n=2 i hydrogen er 10,2 eV. (elektronvolt)
Spørgsmål a, som jeg har regnet ud, lyder sådan her:
Hvor stor er energiforskellen i joule? Jeg har fået det afrundet til 1,63*10-18 Joule.
Problemet er de følgende spørgsmål, som lyder sådan her:
b) Hvilken frekvens har den stråling, der udsendes, når elektroner springer fra tilstand 2 til tilstand 1?
c) Hvilken bølgelængde har strålingen?
og e) Besvar de samme spørgsmål for overgangen fra n=3 til n=2. Her er energiforskellen 1,9 eV.
Det der er mit problem er, at jeg ikke kan finde ud af at regne b) ud uden at kende bølgelængden, hvilket jeg jo ikke gør.
Svar #1
10. februar 2015 af peter lind
Energi = h*f = h*c/λ h er Plancks konstant, f er frekvensen, c er lyshastigheden og λ er bølgelængden
Skriv et svar til: Regne frekvens for stråling på hydrogen.
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.