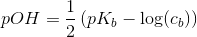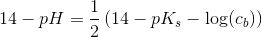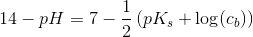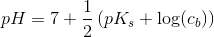Kemi
Butansyreopløsning og Natriumchlorid
Hej, nogen der kan hjælpe med opgave c i vedhæftet dokument.
Hvordan skal jeg gribe opgaven an - jeg er helt blank?
Svar #1
01. maj 2015 af Heptan
Formelt set bliver al syren omdannet til sin korresponderende base.
Du skal altså beregne pH for en opløsning af butanoat, ved at bruge formlen for svage baser:
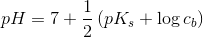
hvor pKs = 4,8
... bemærk at det ikke er en 0,0100 M opløsning længere, da den er blevet fortyndet fra 100 mL til 200 mL.
Svar #2
01. maj 2015 af Tina12453
Okay, men ser formlen for svage baser ikke således ud:
pH= 0,5 *(pKb + log cb )
og hvor kommer 7-tallet fra?
Når opløsningen er fortyndet, er stofmængdekoncentrationen så 0,1 M
Svar #6
01. maj 2015 af Heptan
#2Når opløsningen er fortyndet, er stofmængdekoncentrationen så 0,1 M
Nej, hvis en opløsning fortyndes må stofmængdekoncentrationen jo bliver mindre end den var før.
Skriv et svar til: Butansyreopløsning og Natriumchlorid
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.