Kemi
Reaktionshastighed og hastighedsudtryk
03. januar 2016 af
lokpæø (Slettet)
-
Niveau: B-niveau
Hej, jeg skal definere henholdsvis reaktionshastighed og hastighedsudtryk. Er der nogle der kan hjælpe mig med dette?
Skriv et svar til: Reaktionshastighed og hastighedsudtryk
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.


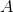 :
:![v=-\frac{\mathrm{d}\left [ A \right ] }{\mathrm{d} t}](https://media.studieportalen.dk/images/equations/FToaJGUNPRpBedqT1Z9N1g==.gif)
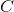 :
:![v=\frac{\mathrm{d}\left [ C \right ] }{\mathrm{d} t}](https://media.studieportalen.dk/images/equations/h-icxBlEWDacNJ_7vvODMw==.gif)
![-\frac{\mathrm{d} [A]}{\mathrm{d} t}=k\cdot [A]^x](https://media.studieportalen.dk/images/equations/XyMnKbDLDEDmXicgO9wZxg==.gif)
![-\frac{\mathrm{d} [A]}{\mathrm{d} t}=k\cdot [A]^0=k](https://media.studieportalen.dk/images/equations/7oS7-puidHLyRATNgaxJzQ==.gif)
![[A]_t=-kt+[A]_0](https://media.studieportalen.dk/images/equations/AD9XzYq-lHFso7z04jgsuA==.gif)
![-\frac{\mathrm{d} [A]}{\mathrm{d} t}=k\cdot [A]](https://media.studieportalen.dk/images/equations/Jyc5hgsWKfkP76KIry7www==.gif)
![[A]_t=[A]_0\cdot e^{-kt}](https://media.studieportalen.dk/images/equations/4p34K57XSwTdliHHpV2V8Q==.gif)
![-\frac{\mathrm{d} [A]}{\mathrm{d} t}=k\cdot [A]^2](https://media.studieportalen.dk/images/equations/LhFPrtStg3VfzyFv9qkjEw==.gif)
![[A]_t=\frac{1}{kt+{[A]_0}^{-1}}](https://media.studieportalen.dk/images/equations/ReelBKSd5dD33C87WikeUg==.gif)